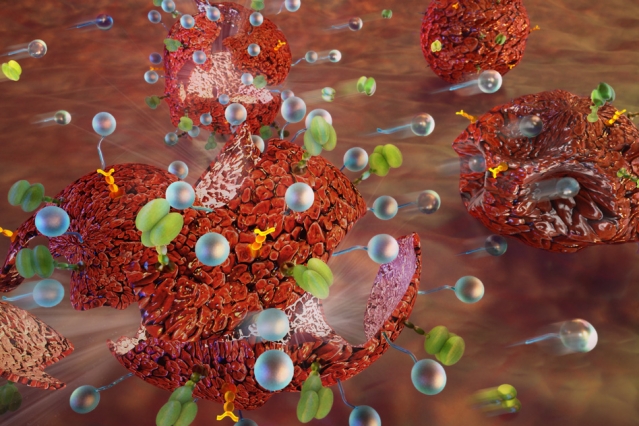
肿瘤表面被“栓”上了像珍珠一样的纳米颗粒~(图片来源:MIT 官网)
1959 年,著名的物理学家 Richard Feynman 在加州技术研究所做了一个演讲,题目为「There’s Plenty of Room at the Bottom」。演讲中他设想了一种非常小的微粒,小到可以在细胞水平控制,这就是纳米颗粒的“雏形”。
随着纳米技术的发展,近年来,越来越多的领域都有了它的身影,其中就包括医学领域。在抗击癌症的研究中,部分科学家把目光放在了纳米颗粒的身上,利用它“卧底吸引免疫系统的火力”,或者是以它为载体,穿过“屏障”递送药物等等。而这一次,来自 MIT 的著名科学家 Robert Langer 教授利用纳米颗粒设计出了一种抗癌新方法!他们的研究发表在昨天的《自然通讯》杂志上 [1]。

Robert Langer 教授(我们给大家介绍过的 MIT 把磨皮功能搬到现实了!科技真心疯了…… | 奇点猛科技的研究就是由 Langer 教授做的,Langer 教授的“高产”实在是让人佩服!)
他们把纳米颗粒“栓”在了肿瘤细胞表面,这样的做法竟然能让诱导细胞凋亡的药物的效力增加 50%,消除了小鼠体内超过 90% 的肿瘤细胞!
听起来简单得难以置信对不对?但这其实是一个大胆的、另辟蹊径的做法。目前很多针对肿瘤的研究都集中在它们异常的遗传特征和生化特性上,但是这个研究则是瞄准了“物理因素”。
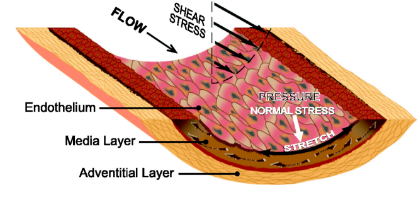
比如说,血液在血管内流动时会对血管内皮细胞产生“撕扯”(专业名词为剪应力,shear stress,是血液流动时施加给血管壁的力),除了血液,其他的体液循环也会对周围的细胞、组织产生这样的撕扯。所以,我们不难推断出,肿瘤细胞在体液循环的过程中也会暴露在“撕扯”中。过去的研究显示,这些“流体”对肿瘤的撕扯会改变肿瘤细胞的信号转导,从而影响肿瘤的生长 [2]。
在这样的环境下,肿瘤也要“为自己打算”,它们会通过增加自身的“硬度”、改变血流量等方法来“让自己过得舒心一些”。基于这样的背景,研究人员们想到,能不能人为地改变一些这样的物理因素,让肿瘤更脆弱,更难以抵抗药物的攻击呢?
在有了这个设想后,他们又选择了一款试验药物 TRAIL,它是肿瘤坏死因子家族的一员,能够结合肿瘤细胞表面的受体,导致肿瘤细胞死亡。在过去的研究中,研究人员已经发现 TRAIL 可以靶向肿瘤细胞,具有治疗实体瘤和转移性肿瘤细胞的潜力 [3]。

第一作者 Michael Mitchell 博士
研究人员首先进行了体外实验,他们选择了结肠、前列腺和乳腺的肿瘤细胞,分别将它们用 TRAIL 处理,然后放置于静态条件和模拟人体的流体环境下。结果显示,暴露在 “剪应力”作用下的三种肿瘤细胞死亡的数量显著增加。研究的第一作者,在 Langer 教授实验室工作的博士后 Michael Mitchell 说,“我们的初步研究表明,肿瘤细胞暴露在剪应力作用下后会对这种药物更加敏感”。
这个结果让研究人员意识到,增加作用于肿瘤细胞上的“力”或许能够让肿瘤细胞更容易被杀死。于是他们想到了一个办法——把纳米颗粒“栓”到肿瘤细胞表面!当血液或者是组织液流动的时候,会“拉动”这些颗粒,但因为颗粒被拴住了,所以纳米颗粒会对肿瘤细胞产生更大力度的“撕扯”,增强力的作用效果。
这让奇点糕想到了一种动物:狗,狗对食物的撕咬能力大家都是知道的,所以 Langer 教授团队的这个想法简直就是塑造了一个“纳米狗”的形象啊!
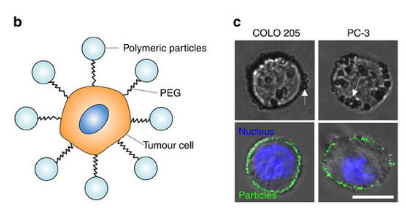
b 为肿瘤细胞与纳米粒子的结合示意图,c 为两种不同的肿瘤细胞系中,纳米颗粒与肿瘤细胞的结合情况,蓝色荧光为肿瘤细胞细胞核,绿色荧光为纳米颗粒
这些纳米颗粒是由可降解的聚乳酸 - 羟基乙酸共聚物(PLGA)做成的,PLGA 具有好的生物相容性且无毒害作用,在临床上已经有应用了。而“栓”着它们的“线”是聚乙二醇(PEG)分子,上面附有特异性的配体可以和肿瘤细胞表面的蛋白结合,这样子它们就不会“错误地降落到”正常细胞表面了。
设计好了纳米颗粒,研究人员再次进行了体外实验。他们准备了从 100nm-1μm 不等的粒子,按大小分组,分别加入到用 TRAIL 处理过的结肠癌和前列腺癌两种细胞系中,可以观察到无论多大的粒子都是只在肿瘤细胞表面“降落”。在同样的流速中,栓上了纳米颗粒的肿瘤细胞的死亡率明显比没有栓的要高!而且实验结果显示,纳米颗粒越大,数量越多,杀死癌细胞的效果就越好。此外,他们也观察到这一策略对健康的细胞是没有产生影响的。
在体外实验表现如此“神勇”的纳米颗粒在体内也能如此吗?于是研究人员继续在小鼠体内做了实验。他们将培养的肿瘤细胞通过尾静脉注射到小鼠体内,15 分钟后注射纳米颗粒,血管内的血液流动能够提供剪应力。在纳米颗粒与肿瘤细胞结合后,研究人员又给小鼠使用了 TRAIL。经过定量分析,他们发现,只注射肿瘤细胞,不做任何治疗的小鼠每毫升血液中约有 40000 个肿瘤细胞,而注射了纳米颗粒和 TRAIL 的小鼠每毫升血液中的肿瘤细胞只有不到 3000!这个方法使得肿瘤细胞减少了大约 92%。
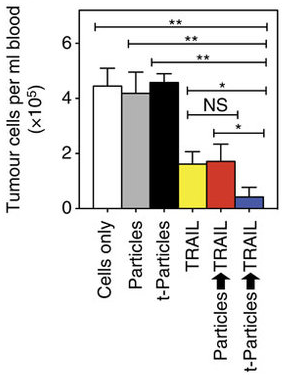
纵轴为每毫升血液中肿瘤细胞的数量,横轴依次为只注射肿瘤细胞、不附有特异性配体的纳米颗粒、附有特异性配体的纳米颗粒、TRAIL、不附有特异性配体的纳米颗粒 +TRAIL、附有特异性配体的纳米颗粒 +TRAIL
除了血液循环中的肿瘤细胞外,研究人员还对已经形成了实体瘤的前列腺癌小鼠进行了治疗。治疗过程中,除了纳米颗粒和 TRAIL,他们还给小鼠使用了白藜芦醇,这是一种天然存在的多酚,具有抗肿瘤活性,已经有研究证明它可以增强 TRAIL 的治疗效果 [4]。在“多方联手”下,与只用 TRAIL 的对照组相比,这些小鼠的实体瘤生长受到了明显的抑制,肿瘤的体积减小了超过 80%!在肿瘤被控制了的同时,小鼠也没有出现食欲降低、体重下降等不良反应,毒理检测也没有看到明显的肝肾毒性。
这样的结果也得到了没有参与研究的科学家的认可,康奈尔大学的生物医学工程教授 Michael King 表示,这个方法太有创意了!他从来没有见过有其他人尝试把纳米颗粒“栓”在癌细胞表面来提高细胞对药物的敏感性。Mitchell 博士也说,他们对这种组合非常感兴趣,接下来还将进一步探索这种方法与其他药物相结合的作用如何。
参考文献:
[1] Mitchell, M. J. et al. Polymeric mechanicalamplifiers of immune cytokine-mediated apoptosis. Nat. Commun. 8,14179 doi: 10.1038/ncomms14179(2017)
[2] Swartz, M. A. & Lund, A. W. Lymphatic and interstitial flow in the tumour microenvironment: linking mechanobiology with immunity. Nat. Rev. Cancer 12, 210–219 (2012)
[3] Mitchell, M. J., Wayne, E., Rana, K., Schaffer, C. B. & King, M. R.TRAIL-coated leukocytes that kill cancer cells in the circulation.Proc. Natl Acad. Sci. USA 111, 930–935 (2014)
[4] Ganapathy,S., Chen,Q., Singh,KP, Shankar,S.&Srivastava,RK Resveratrol enhances antitumor activity of TRAIL in prostate cancer xenografts through activation of FOXO transcription factor. PLoS ONE 5,e15627(2010)
扫描上面二维码在移动端打开阅读