来自弗莱堡大学分子医学和细胞研究所(IMMZ)研究组的蒂尔曼·布鲁默博士、Dr. Florian Weinberg 博士与弗莱堡大学医学中心临床病理和医学系 I 科学家联手已经确定了癌症治疗的新目标。研究人员发现,RIOK1 酶与 RAS 蛋白质合作,RAS 蛋白经常在肿瘤中突变,从而促进肿瘤生长和转移发展。这些继发性肿瘤由原发性肿瘤(如果不及时移除)扩散而来,是大多数癌症患者死亡的原因。研究人员认为可能使用所谓的抑制剂来阻断 RIOK1 的酶活性,从而减缓疾病进展。该小组最近在期刊 EBioMedicine 上发表了研究结果。
癌症疾病的特征在于导致身体自身细胞不受控制生长的基因突变。这反过来导致肿瘤的发展。大多数治疗方法将手术去除与化疗或放射治疗肿瘤结合,两者都用于抑制细胞的快速生长。特异性抑制剂也可用作额外或替代疗法。这些药物抑制肿瘤中突变基因产生的有害蛋白质和酶的活性。然而,目前只有很少的方法专门治疗 RAS 驱动的肿瘤。因为大约有 30%的癌症患者在其肿瘤中携带 Ras 突变,所以非常需要找到靶向针对 RAS 的新方法。
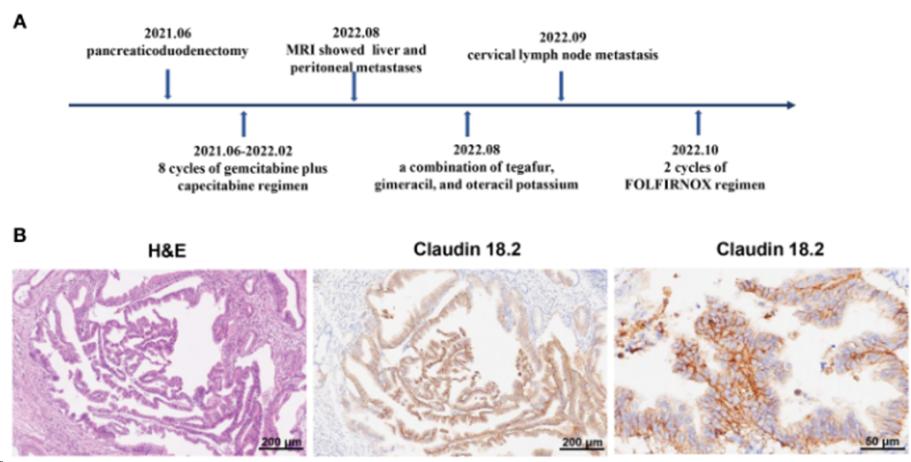
科学家研究人类 RAS 突变的肺癌,乳腺癌和结肠直肠癌细胞在细胞培养和动物模型中的生长行为。在每种情况下,他们都能够遗传修饰细胞,使得它们不再能够产生 RIOK1,这是一种模拟待开发的 RIOK1 抑制剂的作用的方法。通过这种方法,作者能够减少癌细胞的生长和侵袭性。特别是在动物模型中,研究人员观察到修饰的细胞不再能够转移。 RIOK1 属于蛋白激酶的酶家族,其抑制剂已经成功应用于癌症治疗。因此,科学家认为,在不久的将来可以开发出抑制 RIOK1 酶活性的类似物质。此外,RIOK1 可以更准确地预测肺癌和乳腺癌的进展,因为研究人员观察到预后较差的患者肿瘤组织中 RIOK1 的产量增加。
研究人员指出,需要更多的研究来证实 RIOK1 作为癌症治疗的目标。重要的是,例如,了解酶支持癌症生长和转移的确切机制。在临床研究中可以测试药物之前,先对模型生物体测试抑制剂也是至关重要的。研究人员对蛔虫和人类细胞的初步研究已经证明,健康的身体细胞只是部分受到影响,或者完全不受 RIOK1 损失的影响,因为它们不依赖于酶。这意味着,癌细胞将同时被抑制生长和传播新肿瘤。
扫描上面二维码在移动端打开阅读