还记得之前方姨在《来看看怎么像那位老爷子一样在中国治肺癌??》中提到的LOXO各种吊炸天的小分子抗癌候选药物吗?就在今天,FDA批准了LOXO-101上市!
先来看看FDA的原文
The U.S. Food and Drug Administration today granted accelerated approval to Vitrakvi (larotrectinib), a treatment for adult and pediatric patients whose cancers have a specific genetic feature (biomarker).
This is the second time the agency has approved a cancer treatment based on a common biomarker across different types of tumors rather than the location in the body where the tumor originated.
The approval marks a new paradigm in the development of cancer drugs that are “tissue agnostic.”
Vitrakvi is indicated for the treatment of adult and pediatric patients with solid tumors that have a neurotrophic receptor tyrosine kinase (NTRK) gene fusion without a known acquired resistance mutation, are metastatic or where surgical resection is likely to result in severe morbidity and have no satisfactory alternative treatments or that have progressed following treatment.

LOXO-101是一款靶向原肌球蛋白受体激酶(TRK)抑制剂,针对的是NTRK1、NTRK2或者NTRK3基因融合的肿瘤患者,这些基因改变在很多肿瘤中广泛存在,导致TRK信号传导和肿瘤生长失控。
LOXO-101(商品名Vitrakvi)是第一款获批的口服TRK抑制剂,获批的适应症是用于治疗患有NTRK基因融合的局部晚期或转移性实体瘤的成人和儿童患者。
LOXO-101是第二款以某一靶点为适应症获FDA批准的药物(PD-1/L1是第一个作为适应症的靶点),不再以肿瘤位点区分,是抗肿瘤治疗方案从肿瘤生长位置靶向,向肿瘤的基因表达遗传特征靶向的重要转折。

今年2月新英格兰医学杂志(NEJM)在线发表了LOXO-101进行的三项安全性和有效性临床试验数据,分别是成人I期、儿童I-II期,以及青少年和成人II期临床试验(NCT02122913,NCT02637687和NCT02576431)。临床试验结果显示对于年龄为4个月至76岁的患者,针对17种不同癌症治疗总体反应率为75%,非常亮眼的结果。癌症种类包括阑尾癌,乳腺癌,胆管癌,结直肠癌,胃肠道间质瘤(GIST),婴儿纤维肉瘤,肺癌,黑色素瘤,胰腺癌,甲状腺癌等17种肿瘤。
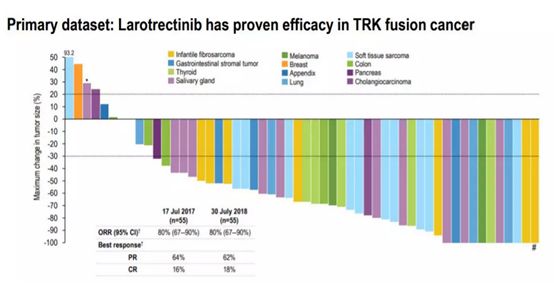
LOXO-101在多种肿瘤类型均显示有效性,因此, 肿瘤患者如果存在NTRK1、NTRK2或者NTRK3基因融合,理论上都是适合的,这一部分患者将看到新的希望。
值得一提的是,在目前免疫抗肿瘤候选药物大热的情况下,LOXO-101是一款小分子化合物。这无疑是给一些认为小分子化合物没有希望的言论最好的反击。小分子化合物的创新药研发,仍然是大有可为的。
向LOXO这家创新药物研发公司表示祝贺(只有35名员工,何时国内才能出现这样的公司??),同时也要向老东家Bayer表示祝贺!Bayer在2017年果断的以4亿首付+4.5亿上市里程碑付款(刀轮)拿下了这款药物的销售权益。短短一年,这笔投资已经有了确定性的回报。

扫描上面二维码在移动端打开阅读





