
文章转自:深圳湾实验室 内容并不代表本网立场!如有侵权请联系管理员删除!
1.小分子化学药物的靶点发现及虚拟筛选
1.1 以2019-nCoV-3CL水解酶为靶标
2020年1月25日,饶子和/杨海涛团队快速表达了2019-nCoV 3CL水解酶(Mpro)并获得了高分辨率晶体结构(PDB ID:6LU7)。同日,中国科学院上海药物研究所和上海科技大学免疫化学研究所抗2019-nCoV病毒感染联合应急攻关团队报道了综合利用虚拟筛选和酶学测试相结合的策略进行药物筛选,发现了30种可能对2019-nCoV有治疗作用的药物、活性天然产物和中药。候选药物包括蛋白酶抑制剂茚地那韦(Indinavir)、沙奎那韦(Saquinavir)、洛匹那韦(Lopinavir)、卡非佐米(Carfilzomib)、利托那韦(ritonavir)等12种抗HIV药物,2种抗呼吸道合胞病毒药物,1种抗人巨噬病毒药物,1种抗精神分裂症药物,1种免疫抑制剂以及2种其他类药物;发现含有“二苯乙烯”结构的孟鲁司特以及植物药活性成分虎杖苷和脱氧土大黄苷与Mpro结合较好,可能对病毒有抑制作用;在前期抗SARS研究及计算机模拟基础上发现老药肉桂硫胺、环孢菌素A可能对2019-nCoV有效,其中肉桂硫胺是上世纪70年代用于抗精神分裂症的药物,对冠状病毒3CL水解酶具有抑制作用,免疫抑制剂环孢菌素A可以阻止病毒的核衣壳蛋白与人的环孢亲和素A相互结合,已有研究表明联用干扰素和环孢菌素A能显著抑制冠状病毒在人类支气管和肺部复制及造成的组织损伤。他们研究还发现,虎杖、山豆根等中药材中可能含有抗2019-nCoV有效成分。(请参考:http://www.simm.cas.cn/xwzx/kydt/202001/t20200125_5494417.html )
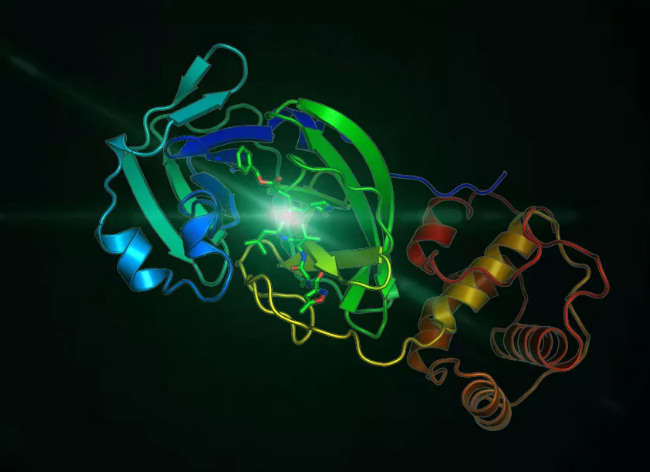
图1. 2019-nCoV 3CL水解酶(Mpro)晶体结构
1.2 以2019-nCoV-PLP蛋白酶为靶标
研究表明,冠状病毒nsp3编码的木瓜样蛋白酶(papain-like protease,PLP)在病毒基因组复制及逃避宿主抗病毒天然免疫中发挥重要作用,是冠状病毒感染人类所必需的重要蛋白,也是药物开发的良好靶点。2020年1月28日华中科技大学李华教授等组成的联合攻关小组发现2019-nCoV蛋白序列中2019-nCoV-PLP序列与SARS-CoV-PLP具有86%的氨基酸同源性。因此,他们使用同源建模的方法模拟了2019-nCoV_PLP的蛋白质结构,明确了它的药物结合口袋,运用基于蛋白质结构的计算机虚拟筛选方法,从化合物库中筛选得到33个2019-nCoV_PLP的潜在抑制剂。(请参考:http://news.hust.edu.cn/info/1002/37436.htm )
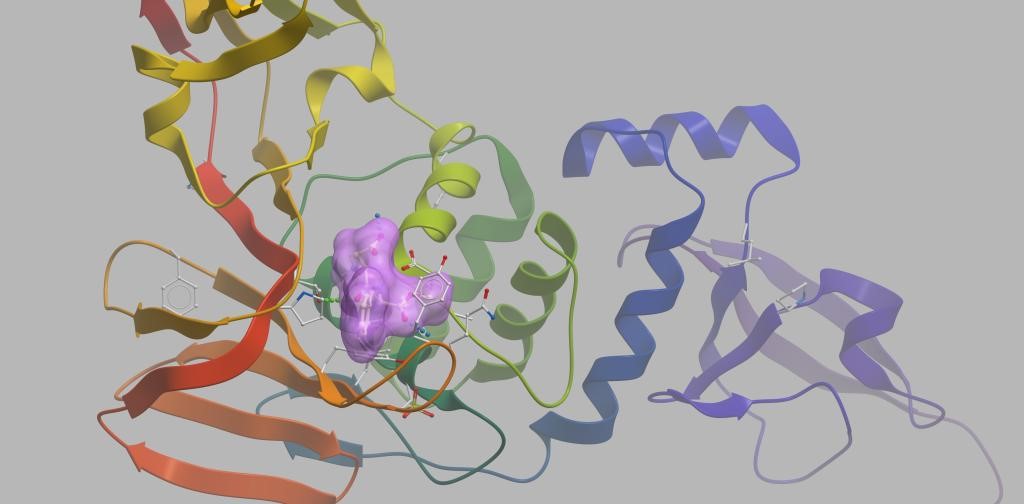
图2. 潜在的抑制剂与2019-nCoV_PLP结合示意图。
1.3 以血管紧张素转化酶ACE2为靶标
2020年1月21日,中国科学院上海巴斯德研究所郝沛研究员等合作于SCIENCE CHINA Life Sciences(《中国科学:生命科学》英文版)期刊在线发表的通讯文章使用计算机模拟的方法发现了,2019-nCoV的S-蛋白的受体结合结构域(RBD)与人血管紧张素转化酶ACE2的结合作用较强。他们认为S-蛋白-ACE2结合通路可能是武汉新型冠状病毒具有较高公共卫生风险的原因之一。因此,ACE2也可能用于2019-nCoV的治疗研究。(请参考:http://engine.scichina.com/publisher/scp/journal/SCLS/doi/10.1007/s11427-020-1637-5?slug=fulltext)
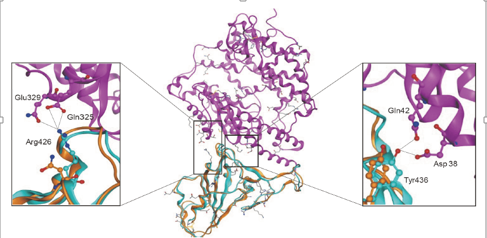
图3. 与人ACE2分子(品红色带)相互作用的2019-nCoV S-蛋白的结构模型。中图:2019-nCoV S-蛋白(棕色带)与SARS-nCoV S-蛋白(浅蓝色带)的结构重叠。左图:显示了该区域中S蛋白中的Arg426与ACE2中的Gln325 / Glu329之间的氢键相互作用。右图:显示了S蛋白中Tyr436与ACE2中Asp38 / Gln42之间氢键相互作用的区域。
2 已知药物的使用
2.1 小分子药物
2020年1月24日,武汉金银潭医院黄朝林根据2019年12月16日至2020年1月2日的41名患者的临床数据发表文章报道了洛匹那韦/利托那韦片(Lopinavir/ritonavir,LPV/r,商品名:克力芝)联合治疗2019-nCoV感染的肺炎的随机对照试验。根据过往洛匹那韦/利托那韦片对SARS-CoV感染的患者有“实质性的临床益处”的结果推测,这种疗法可能对2019-nCoV感染的患者有效。[1](请参考:The Lancet 2020, https://doi.org/10.1016/S0140-6736(20)30183-5)目前,国家卫健委已将治疗艾滋病药物洛匹那韦/利托那韦片纳入《新型冠状病毒感染的肺炎诊疗方案(试行版)》。
2020年1月27日,美国Science期刊刊登了一篇评论称,由Gilead(吉利德制药)开发的抗埃博拉病毒药物Remdesivir (GS-5734)可能更适合冠状病毒的治疗。该药物目前仍处于临床阶段,是一种病毒聚合酶的抑制剂。同时,他们也指出使用该类药物与单克隆抗体联合用药的效果可能最佳。(请参考:https://www.sciencemag.org/news/2020/01/can-anti-hiv-combination-or-other-existing-drugs-outwit-new-coronavirus )
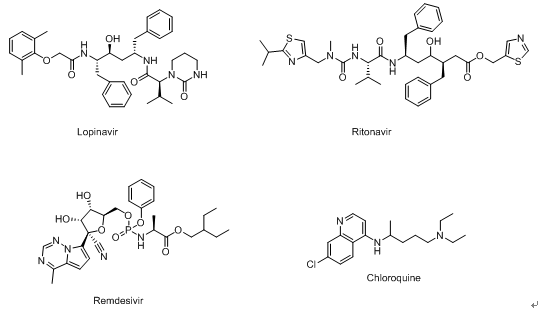
图4. 近日报道的几种对2019-nCoV可能有效的几种药物
2020年1月28日,武汉病毒研究所与军事医学科学院毒物药物研究所联合报道了在细胞层面上对2019-nCoV有较好抑制作用的Remdesivir、氯喹(Chloroquine,Sigma-C6628)、利托那韦(Ritonavir)等三种已知药物。(请参考:http://www.cas.cn/zt/sszt/kjgzbd/mtbd/202001/t20200129_4732980.shtml )
2.2 单克隆抗体
2020年1月28日,复旦大学应天雷等在bioRxiv在线发表的一篇文章中比对2019-nCoV和SARS-nCoV的S-蛋白的RBD相似度为73%,因此已发现的SARS-nCoV抗体可能可以用于治疗2019-nCoV。他们通过比较多种SARS-nCoV单克隆抗体与2019-nCoV RBD结合的亲和力,发现CR3022抗体具有明显的结合,证明了这种抗体可能可以作为预防和治疗2019-nCoV的候选药物。[2](请参考:bioRxiv 2020,doi: https://doi.org/10.1101/2020.01.28.923011 )
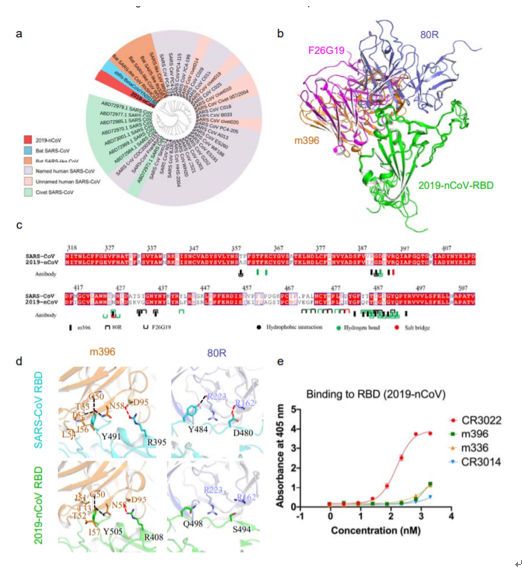
图5. (a)从其蛋白质BLAST序列进行的2019-nCoV穗状糖蛋白的系统发育分析;(b)2019-nCoV RBD与SARS-CoV RBD特异性抗体(m396、80R和F26G19)结合的计算机模拟结构图;(c)2019-nCoV RBD和SARS-CoV RBD的蛋白质序列比对,只显示参与SARS-CoV特异性抗体相互作用的主要残基;(d)比较计算机模拟的SARS-CoV-RBD和SARS-CoV-RBD特异性抗体的结合模式(第一行)和2019-nCoV-RBD和SARS-CoV-RBD特异性抗体的结合模式(第二行);(e)通过酶联免疫吸附测定(ELISA)确定单克隆抗体与2019-nCoV RBD的亲和力。
3 疫苗研究进展
据新华社报道,美国医学专家正与中国同行合作研发针对新型冠状病毒的疫苗。美国休斯敦贝勒医学院(Baylor College of Medicine)教授Peter Hotz通过电子邮件表示,贝勒医学院正在与美国得克萨斯大学、美国纽约血液中心以及中国上海复旦大学合作开发疫苗。他表示,这是一项很好的国际合作,但疫苗研发需要时间。(请参考:http://m.xinhuanet.com/2020-01/23/c_1125497398.htm)
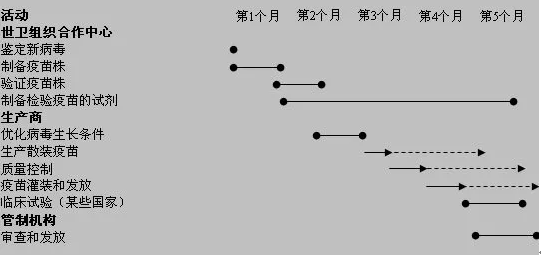
图6. 疫苗制作时间周期
(图片来源:https://www.who.int/csr/disease/swineflu/notes/h1n1_vaccine_20090806/zh)
参考文献
[1] C. Huang, Y. Wang, X. Li, L. Ren, J. Zhao, Y. Hu, L. Zhang, G. Fan, J. Xu, X. Gu, Z. Cheng, T. Yu, J. Xia, Y. Wei, W. Wu, X. Xie, W. Yin, H. Li, M. Liu, Y. Xiao, H. Gao, L. Guo, J. Xie, G. Wang, R. Jiang, Z. Gao, Q. Jin, J. Wang, B. Cao, Clinical features of patients infected with 2019 novel coronavirus in Wuhan, China. The Lancet 2020.
[2] X. Tian, C. Li, A. Huang, S. Xia, S. Lu, Z. Shi, L. Lu, S. Jiang, Z. Yang, Y. Wu, T. Ying, Potent binding of 2019 novel coronavirus spike protein by a SARS coronavirus-specific human monoclonal antibody. bioRxiv 2020.
扫描上面二维码在移动端打开阅读








