近日,在胸部肿瘤学杂志(JTO)上公布的最新研究中,德国默克(Merck KGaA)的在研新药M7824公布的最新临床数据引起轰动!这是一款在研的双功能性免疫疗法,能同时靶向PD-L1通路和TGF-ß通路,有望唤醒和恢复机体的抗肿瘤反应,从而起到控制肿瘤生长的效果。
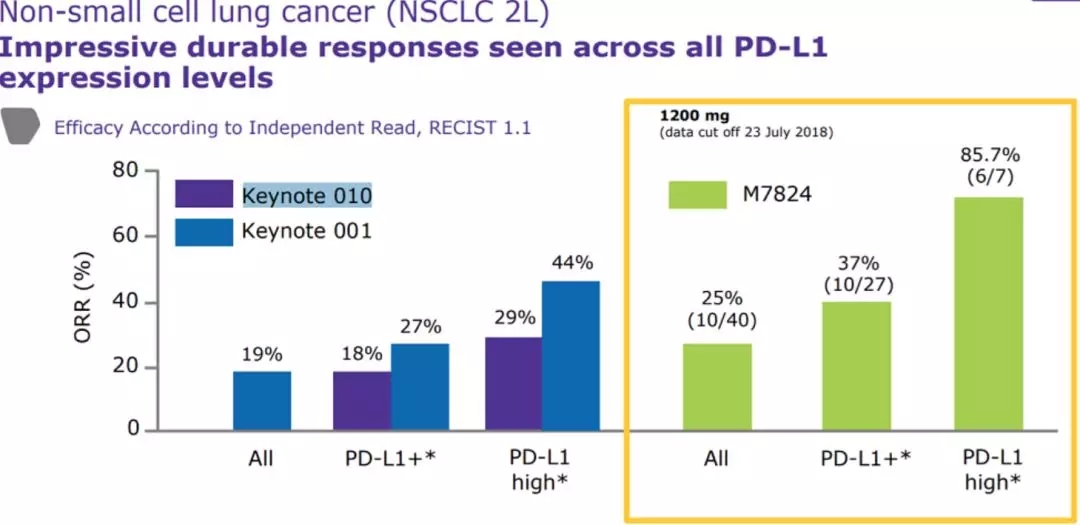
此次更新的数据显示,在非小细胞肺癌患者群体中,这款创新疗法取得了卓越的临床效果——在PD-L1阳性患者群体(PD-L1不小于1%)中,该新药的总体缓解率(ORR)达到了37%。而在PD-L1高表达的患者群体(肿瘤细胞PD-L1表达≥80%中,M7824的客观缓解率(ORR)更是高达85.7%!

国家肿瘤研究中心(NCI)和约翰·霍普金斯医学院(JHMI)两组独立工作的研究人员开发了一种药物
提高应答率,甚至有望适应对常规免疫疗法无效的肿瘤!
Y-TRAP
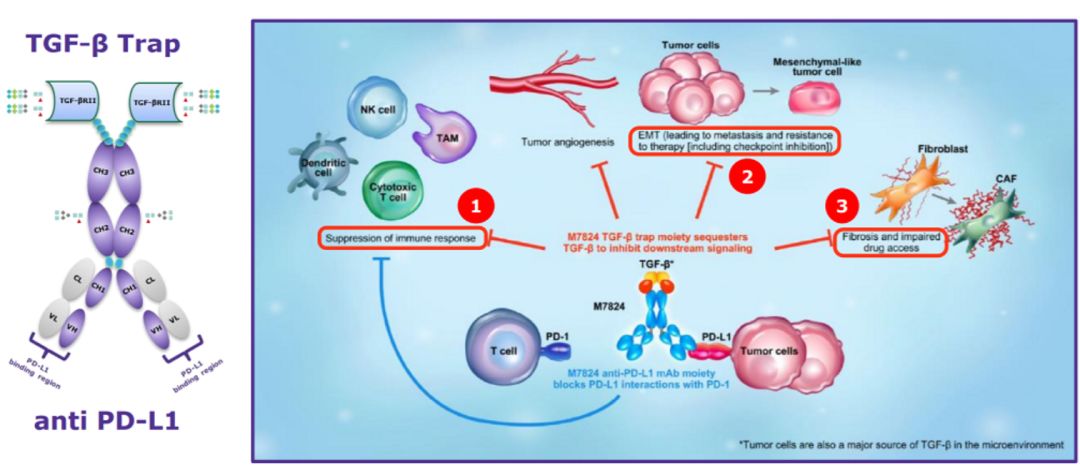
该方法使用的药物Bintrafusp alfa,也就是大名鼎鼎的M7824,是德国默克公司研发的一种双功能抗体蛋白,意味着一个药物可以同时有两个靶点,能同时拮抗TGFβ与PD-L1,这样就会极大地提升药物的有效率,并降低联合用药的副作用。它长这个样子:
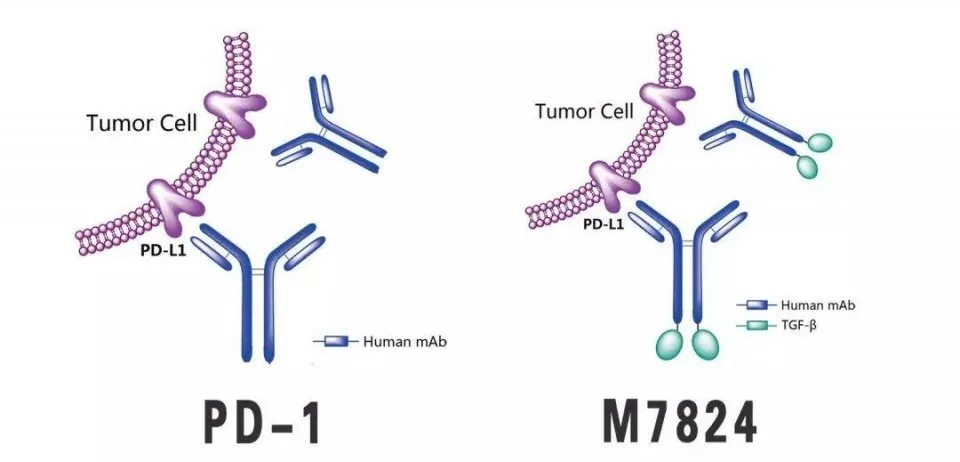
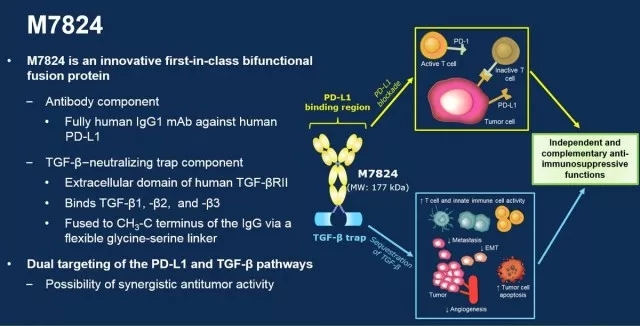
M7824是由人IgG 1组成的双功能蛋白抗PD-L1抗体通过接头与两个TGF-β受体II分子融合
M7824或可比作是第二代PD-1!
这个药物在临床前动物实验的有效率是100%!
全部的试验动物都产生治疗应答!
我们都知道近两年免疫检查点抑制剂已经在各类实体肿瘤的治疗中取得了令人印象深刻的成绩,然而,不幸的是,对这种治疗响应的幸运儿仅有20%,大部分的患者只能与“治愈”的希望失之交臂。
为了让更多的患者对这些免疫疗法产生响应,很多试验正在评估抗PD-1 / PD-L1药物与其他免疫疗法的结合。但是,这些联合策略具有局限性,包括累加毒性等。
M7824双功能抗体代表了一种新兴且令人兴奋的新治疗策略,这种药物可能完美的规避传统免疫疗法的局限性。暨达到双药连用的效果,而不产生更多的副作用,可谓是一箭双雕,鱼与熊掌可兼得。
M7824(MSB0011359C)是一种创新的双功能融合蛋白,由针对PD-L1的人IgG1单克隆抗体组成,融合至TGFβ受体II(TGF-βRII)的胞外域,以充当TGFβ“陷阱”。M7824的抗PD-L1部分其实就是已经获批的免疫检查点抑制剂avelumab(巴文西亚),该药物已在多个国家/地区被批准用于治疗转移性默克尔细胞癌;在美国已被批准用于治疗在铂-或-铂类药物治疗期间或之后进展的局部晚期或转移性尿路上皮癌;与奥西替尼英文联合一线治疗晚期肾细胞癌。
临床前研究已经证实了PD-L1和TGFβ途径之间可能存在互补相互作用,还显示出M7824(而非抗PD-L1抗体)具有逆转癌细胞的间充质化和增强对化疗反应的能力,它的双重抑制可增强抗肿瘤活性。重要的是,在肿瘤微环境中同时靶向PD-L1和TGFβ对那些免疫排斥和免疫冷肿瘤也有效果。
01 PD-L1≥80%,肺癌有效率高达85.7%
在本次更新的肺癌数据是基于NCT02517398Ⅰ期临床试验,纳入的80例晚期非小细胞肺癌患者先前都接受过铂类辅助或新辅助化疗,结果显示,总的客观缓解率(OR)为21.3%(n = 17/80),其中500 mg剂量和1200 mg剂量,ORR分别为17.5%(n = 7/40)和25.0%(n = 10/40)。
值得一提的是在1200 mg剂量下,PD-L1阳性患者客观缓解率达到36.0%(n = 10/27),而对于PD-L1强表达(肿瘤细胞表达≥80%)的患者的客观缓解率高达85.7%(n = 6/7)。
这张图也很清晰的展示了派姆单抗两项研究中的有效率(左)和M7824的对比。
02 广谱抗癌新星,首次人体试验证实对多种实体瘤有效!
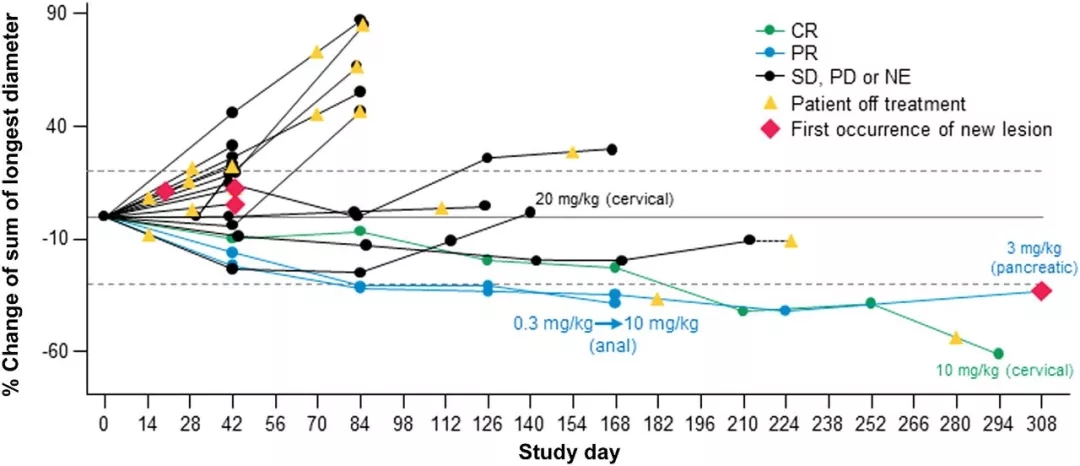
除了非小细胞肺癌,这款抗癌新药像PD-1一样,显示出广谱的抗癌潜力,在首次人体试验的I期临床研究中(NCT02517398),纳入19名晚期实体瘤患者接受了每三周1次,3次或10次20mg/kg的M7824,直至病情进展或不可接受的毒副反应。
根据RECIST v1.1,与基线相比肿瘤病灶的最大变化
结果显示,M7824在所有剂量水平中均有疗效!
包括一例完全缓解的宫颈癌,两个持久的持久缓解的胰腺癌和肛门癌,一例部分缓解宫颈癌,两例病情稳定(胰腺癌;类癌),以及先前进展的晚期肿瘤治疗后出现缩小的病例(脊索瘤)。有趣的是,完全缓解的子宫颈癌和部分缓解的肛门癌均为HPV阳性,而部分缓解的胰腺癌患者存在错配修复缺陷。
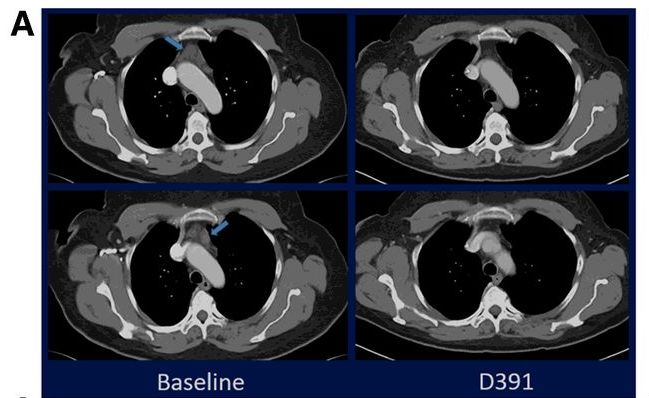
1、宫颈癌患者达到了确认的持续完全应答(完全缓解就是影像学检查所有病灶都消失了)!
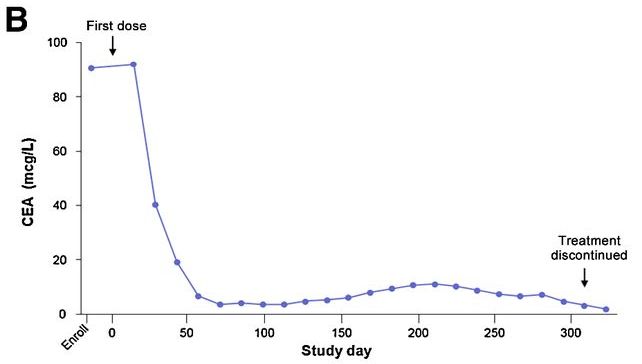
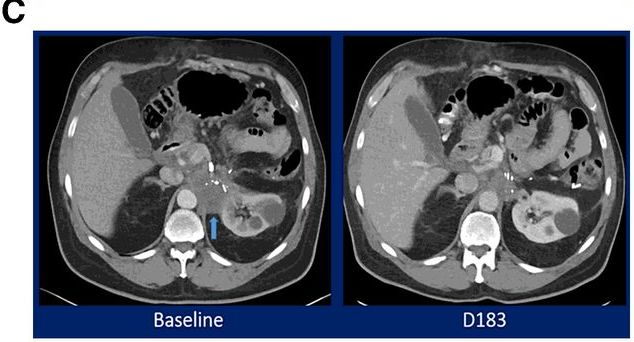
49岁HPV感染阳性的女性转移性宫颈癌患者,在接受顺铂/紫杉醇后加贝伐单抗治疗,随后病情进展,出现两个病理性扩大的纵隔淋巴结(图左侧箭头)。入组M7824的临床试验后,在用药7.5个月后奇迹出现,CT扫描显示达到完全缓解,在13个月的再次扫描仍未发现病灶,证明反应是持久的(图的右侧)。CEA持续下降!
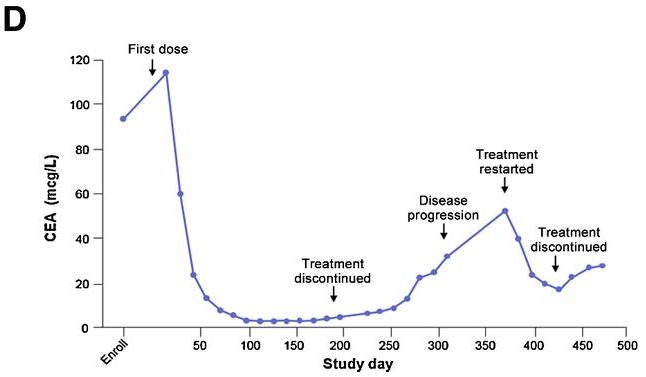
这位61岁的男性患有局部晚期错配修复缺陷型胰腺癌的患者,化疗后入组M7824的临床试验,治疗3个月的CT扫描显示部分缓解,4.5个月时仍显示部分缓解(30%),半年后CT扫描显示病灶竟缩小49%!CEA持续下降!
此外,M7824也在类癌、绒毛膜瘤等罕见癌症中显示出令人鼓舞的治疗效果!整体安全可控,下一步扩展队列的临床实验已经在进行。全球肿瘤医生网将密切关注,跟踪报道!
研究的初步数据表明,当以1-20mg / kg的剂量施用时,M7824通常具有良好的耐受性,并且表明该药物可以结合PD-L1并且还阻断TGF-β信号传导,证实了该化合物的临床活性。此外还发现M7824可起到持续的完全反应,持续的部分反应。
临床试验目前仍在美国,英国,加拿大,澳大利亚,欧洲,韩国,台湾和日本招收患者。
此外,另一项与该项目相同且开放标签的1期临床试验(NCT02699515)也正在进行中,但仅限于日本,台湾和韩国,并且不再招募。
国立癌症研究所开展的2期临床试验(NCT03315871)也将评估M7824作为联合治疗的效果。该试验的目的是验证Prostvac,CV301和M7824 的组合是否可以诱发复发性前列腺癌患者的抗肿瘤反应。该研究将在美国进行,但尚未公开招募患者。
以上临床试验详细信息可自行在https://clinicaltrials.gov/查询,也可致电全球肿瘤医生网医学部咨询,400-666-7998.
http://clincancerres.aacrjournals.org/content/24/6/1287
https://immuno-oncologynews.com/io-m7824/
https://immuno-oncologynews.com/2018/03/27/new-y-
https://www.ncbi.nlm.nih.gov/pmc/articles/PMC7057416/
https://www.merckgroup.com/investors/events-and-presentations/webcasts-and-presentations/2019/en/190205-M7824-presentation.pdf

扫描上面二维码在移动端打开阅读