前 言
5月14日,2020ASCO年会公布了会议摘要,除了LBA外,大部分研究的摘要都已经出炉。今年大会将于2020年5月29号至6月2号正式召开在线虚拟会议。大会上报道的研究琳琅满目,新方案屡见不鲜,许多我们期待的研究都公布了具体数据。在肺癌中,新靶点药物、新双靶组合和免疫新疗法更是花样百出。小编今天挑出非小细胞肺癌(NSCLC)、小细胞肺癌(SCLC)、消化道肿瘤(肝胆食管胃肠)和乳腺癌等主要癌种的重点数据,进行分享。
非小细胞肺癌
一、靶向篇
1. EGFR
贝伐单抗+厄洛替尼一线治疗EGFR突变NSCLC的最终生存分析:NEJ026(摘要号9506,口头报道)
NEJ026: Final overall survival analysis of bevacizumab plus erlotinib treatment for NSCLC patients harboring activating EGFR-mutations.
NEJ026 III期研究纳入EGFR突变NSCLC患者,一线使用厄洛替尼+贝伐单抗vs厄洛替尼进行治疗,既往公布了PFS得到延长的阳性结果,这次报道了OS。结果显示,两组的中位OS分别为50.7(联合组) vs 46.2(单药组)个月,OS无差异(HR=1.00)。两组分别有25.9%(联合组)及23.2%(单药组)在二线接受奥希替尼治疗,两组的中位PFS2(从入组到二线治疗疾病进展)为联合组28.6 vs 单药组24.3个月。二线治疗中,奥希替尼的中位OS优于化疗(50.7 vs 40.1个月)。综上,EGFR-TKI+抗血管生成药虽然可延长PFS,但却未能转化成长期生存获益。
RELAY+研究:雷莫芦单抗+吉非替尼一线治疗EGFR突变NSCLC的探索性研究(摘要号9564)
RELAY+: Exploratory study of ramucirumab plus gefitinib in untreated patients (pts) with epidermal growth factor receptor (EGFR)-mutated metastatic non-small cell lung cancer (NSCLC).
既往的RELAY研究使用雷莫芦单抗+厄洛替尼一线治疗取得了PFS延长,本次报道的RELAY+研究探索吉非替尼+雷莫芦单抗一线治疗东亚EGFR突变人群的疗效。共纳入了82例患者,1年的PFS率为65%,19del和L858R分别为67.2%和63.4%。ORR为70.7%,DCR为98.8%,中位DOR未达到。9例进展的患者中,有7例检测出T790M突变。
TKI±积极局部放疗一线治疗EGFR突变寡转移NSCLC:III期开放性随机SINDAS研究(摘要号9508,口头报道)
First-line tyrosine kinase inhibitor with or without aggressive upfront local radiation therapy in patients with EGFRm oligometastatic non-small cell lung cancer: Interim results of a randomized phase III, open-label clinical trial (SINDAS)
这是一项国内的III期临床研究,在一线使用EGFR-TKI±积极局部放疗(针对所有的寡转移病灶)治疗EGFR突变NSCLC有寡转移的患者。中期分析共纳入了133例患者,其中51.1%接受了立体定向放疗。随访时间19.6个月,TKI+放疗组的中位PFS显著延长(20.2 vs 12.5个月,P<0.001)。两组的中位OS为25.5 vs 17.4个月(HR=0.6824,P<0.001),差异显著。安全性方面,两组的不良反应发生率相似,都无5级或死亡相关AE。3/4级AE包括肺炎(7.3% vs 2.9%,P>0.05)和食管炎(4.4% vs 3.0%,P>0.05),放射性炎症虽然有增高,但是无差异。这项研究强调了对于晚期患者,放疗同样拥有很重要的治疗地位。
JNJ-372(Amivantamab),EGFR/MET双特异抗体,治疗EGFR20ins突变晚期NSCLC(摘要号9512)
Amivantamab (JNJ-61186372), an anti-EGFR-MET bispecific antibody, in patients with EGFR exon 20 insertion (exon20ins)-mutated non-small cell lung cancer (NSCLC)
JNJ-372为目前获得FDA授予突破性疗法治疗20ins的药物。该药物为EGFR/MET双抗。这次公布了研究数据更新。截至2019.10.30,共有39例EGFR 20ins患者可评估疗效,其中有29例患者接受过铂类化疗,既往中位治疗线数为1。总ORR为36%,接受过化疗患者的ORR为41%。总人群的临床获益率(CR/PR/SD≥11周)为67%。中位PFS为8.3个月,用过铂类化疗患者的PFS为8.6个月。
奥希替尼160mg治疗EGFR20ins:ECOG-ARCIN 5162(摘要号9513)
ECOG-ACRIN 5162: A phase II study of osimertinib 160 mg in NSCLC with EGFR exon 20 insertions
奥希替尼作为三代药,治疗20ins国内外都报道过不少成功案例,这次大会终于公布了该药加量后治疗EFGR 20ins的II期研究数据。该单臂研究显示,21例既往中位治疗线数为2的患者接受了奥希替尼160mg治疗,在20例可评估患者中,ORR为25%(包括1例CR),DCR达到85%。中位PFS为9.7个月,中位DOR为5.7个月。对于TKI治疗预后不佳的20ins,奥希替尼后线治疗展现不错的疗效。
奥希替尼治疗未经过放疗的中枢神经系统转移的携带EGFR突变的非小细胞肺癌患者的II期研究:OCEAN研究。(摘要号9597)
A phase II study of osimertinib for patients with radiotherapy-nave CNS metastasis of non-small cell lung cancer harboring EGFR mutations: The OCEAN study (LOGIK 1603/WJOG 9116L).
OCEAN研究为两个队列的II期研究,包含65个未经放射学治疗的中枢神经系统转移的EGFR突变阳性的非小细胞肺癌患者。患者每日用奥希替尼80mg治疗。在这个报告里, 我们呈现T790M队列的结果。
在2016年10月到2019年7月之间,40名参与者被招募到T790M队列。中位年龄为66.5岁,30%为男性。8名患者为有症状的中枢神经系统转移,大部分患者为多种多样的中枢神经系统转移 (77.5%).中位PFS为7.1个月,ORR为40.5%.
艾氟替尼(AST2818)治疗T790M突变阳性的非小细胞肺癌患者的疗效和安全性:一个多中心的单臂IIb阶段研究(摘要号:9602)
Efficacy and safety of alflutinib (AST2818) in patients with T790M mutation-positive NSCLC: A phase IIb multicenter single-arm study.
方法: 局晚期或转移性EGFR T790M突变的非小细胞肺癌患者,在第一/第二代EGFR-TKI治疗后进展或原发性EGFR T790M突变阳性的患者接受艾氟替尼 80mg 口服 每日一次治疗。 每天集会一次。
结果: 从2018年6月4日到2018年12月8日,有220个患者登记,中位年龄为61岁。所有的患者都有EGFR T790M突变。截止到2019年4月12日,客观缓解率(ORR)为73.6% (95% CI 67.3–79.3). 估计的6周和12周的疾病控制率(DCR) 分别为87.3% 和 82.3% . 中位 PFS 为7.6 个月(95% CI 7.0–NA). 中位总生存(OS)和持续反应时间(DOR)未达到。
Lazertinib治疗EGFR-TKI耐药的NSCLC的颅内抗癌活性,以及治疗T790M的疗效(摘要号9571,9572)
Intracranial anti-tumor activity of lazertinib in patients with advanced NSCLC who progressed after prior EGFR TKI therapy: Data from a phase I/II study
Lazertinib(YH25448)是一种高选择性不可逆的第三代EGFR-TKI,可抑制EGFR19/21突变及T790M突变。I/II期研究纳入了EGFR-TKI治疗失败的181例患者,其中64例在基线就有脑转移(86%为T790M阳性)。结果显示,颅内DCR为90.6%,颅内PFS未达到。在可评估疗效的脑转移人群中,共纳入22例患者,颅内ORR和DCR分别为54.5%和90.9%。
另外,该研究分析了76例T790M阳性患者的疗效。ICR评估的ORR为57.9%,DCR为89.5%,中位PFS为11个月,中位DOR为13.8个月。研究者评估的ORR/DCR/PFS和DOR为72.4%/94.7%/13.2个月/11.8个月。
Nazartinib(EGF816)一线治疗EGFR突变NSCLC的II期研究(摘要号9574)
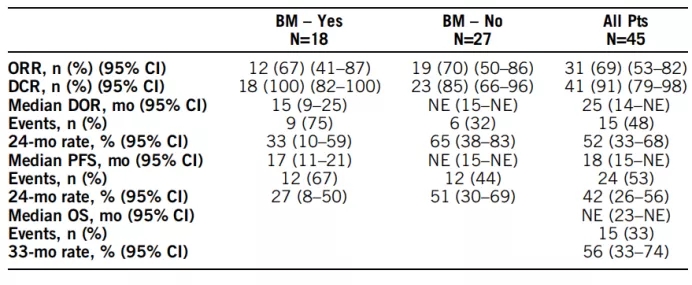
Nazartinib是第三代EGFR-TKI,这次报道了I/II期一线治疗EGFR突变的研究结果。共纳入了45例患者。BIRC评估的ORR为69%,DCR为91%,中位PFS为18个月,中位OS未达到,33个月的OS率为56%。对于脑转移患者,Nazartinib也展现了不错的疗效,如下表。
安罗替尼联合埃克替尼一线治疗EGFR突变晚期NSCLC:ALTER-L004(摘要号9573)
Study of anlotinib combined with icotinib as the first-line treatment in non small cell lung cancer (NSCLC) patients harboring activating EGFR mutations (ALTER-L004).
安罗替尼是正大天晴研发的抗血管口服药。这项前瞻性单臂研究纳入了35例患者,使用安罗替尼12mg(1-14天)+埃克替尼(125mg,tid)进行治疗。结果显示,30例可评估疗效患者的ORR为59%,DCR为88%。其他数据未公布。安全性可管理。期待双口服靶向药在一线的今后走向。
波奇替尼在EGFR20ins经治亚组中的活性。(摘要号9514)
Poziotinib shows activity and durability of responses in subgroups of previously treated EGFR exon 20 NSCLC patients.
此次ASCO公布波奇替尼治疗经治EGFR20ins的亚组疗效。115例患者入组,既往中位治疗线数为2。实际治疗人群的ORR为14.8%,DCR为68.7%。在可评估患者中,ORR为19.3%,未确认的ORR为25%。2线治疗ORR为14%,≥3线治疗ORR为16.2%。
ERBB2 16号外显子跳跃是EGFR-TKI新的耐药机制(摘要号9528)
Exon-16-skipping ERBB2 (ERBB2 Ex16) as a novel resistance mechanism against EGFR tyrosine kinase inhibitors in non-small cell lung cancer (NSCLC).
这是一项国内的研究,一共分析了38680例中国肿瘤患者的肿瘤组织或cfDNA的NGS结果。结果显示,16例患者有ERBB2 16外显子突变,包括11例NSCLC,2例结直肠癌,2例胃癌和3例其他。发生率为0.047%(18/38680)。在11例NSCLC患者中,有9例合并EGFR突变(19del/21L858R)并且既往接受过EGFR-TKI治疗,其中2例有T790M突变。进一步分析显示,3例患者在EGFR-TKI治疗时出现ERBB2 16突变,提示EGFR-TKI治疗与该突变密切相关,可能是潜在的耐药机制。
2.ALK/ROS1
布加替尼治疗日本ALK阳性NSCLC经治患者:J-ALTA(摘要号9537)
Brigatinib in Japanese ALK positive NSCLC patients previously treated with ALK tyrosine kinase inhibitors: J-ALTA
此次ASCO报道了一项II期前瞻性研究,评估布加替尼治疗阿来替尼耐药(无论是否接受过克唑)ALK阳性患者的疗效,以及既往接受过2种ALK-TKI治疗患者的疗效。一共纳入了72例患者,其中47例接受过阿来替尼,使用布加替尼治疗的ORR为30%,中位DOR为6.1个月,中位PFS为7.3个月。颅内ORR为25%。在出现ALK二次突变(耐药性突变)的患者中(包括G1202R,I1171N,V1180L和L1196M),布加替尼也展现了抗癌活性。同是二代ALK-TKI,布加替尼用在阿来替尼耐药后却能展现不错的效果,为ALK患者带来新的保底治疗选择。
TQ-B3139,新型ALK-TKI,治疗中国ALK/ROS1阳性NSCLC的I期研究(摘要号9585)
TQ-B3139是ALK-TKI,其活性比克唑替尼高3-7倍。这项1期研究中,纳入63例既往治疗失败的NSCLC患者。其中59例ALK+,4例ROS1+,有16例患者既往接受过ALK-TKI治疗(11例克唑,5例恩沙替尼),36.5%有脑转移。总体ORR达到73%,DCR为85.7%,中位PFS为12.1个月。脑转移患者的脑病灶ORR为80%(8/10)。未接受过ALK-TKI治疗患者的中位PFS未达到,接受过ALK-TKI患者的PFS为5.6个月。
劳拉替尼在只有脑部进展的ALK阳性肺癌患者中的II期研究(摘要号9595)
A phase II study of lorlatinib in patients (pts) with ALK-positive (ALK+) lung
cancer with brain-only progression.
在2016年11月至2019年1月期间,22个用ALK TKI治疗后有颅内进展的患者在没有其他可测量疾病位点的基础上参与到两个研究机构研究中。患者接受了初始剂量为100mg ,每日的劳拉替尼治疗。
结果: 在参与的22个患者中,在使用2代AIL TKI后,21个患者(95%)出现了疾病进展,14个患者(64%)之前接受过中枢神经系统放射治疗。之前接受过ALK TKI治疗的中位线数为2. 截止到19年12月15日的数据截止日,中位随访时间为14个月。在12周时,颅内疾病控制率为95%,包括8位患者疾病稳定。最佳颅内客观缓解率为59%,伴随6例患者完全缓解,7例患者部分缓解。9例患者 (41%)在研究中再度恶化,包括3例只有颅内感染的患者,5例只有颅外进展的患者,和1例结合再度恶化的患者。4例只有颅外进展的疾病超进展患者继续治疗。由于只有几个进展事件,尽管中位颅内疾病控制率和无进展生存期不是值得尊敬的, 颅内12个月无进展率仍达到81%(95% CI: 53%-94%).
阿来替尼vs克唑替尼一线治疗ALK+的ALEX研究OS更新(摘要号9518)
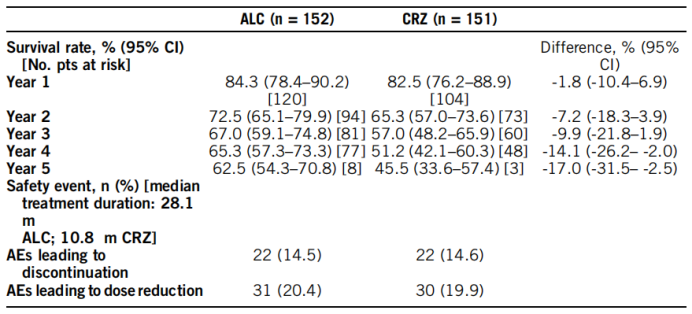
Updated overall survival (OS) and safety data from the randomized, phase III ALEX study of alectinib (ALC) versus crizotinib (CRZ) in untreated advanced ALK+ NSCLC
ALEX研究既往报道过PFS,此次报道了5年的OS结果。中位随访时间为48.2个月,阿来替尼组的中位OS未成熟,克唑替尼组为57.4个月。两组5年生存率为62.5% vs 45.5%。对于基线有脑转移患者,OS的HR为0.58,无脑转移患者的HR为0.76。
劳拉替尼治疗晚期ALK和ROS1阳性的非小细胞肺癌患者:在 IFCT-1803 LORLATU EAP队列的疗效和治疗序列。(摘要号:9615)
Lorlatinib for advanced ALK and ROS1+ non-small cell lung cancer (NSCLC): Efficacy and treatment sequences in the IFCT-1803 LORLATU expanded access program (EAP) cohort.
我们报告了从2015年10月到2019年10月期间,参与法国的劳拉替尼的EAP的晚期,难治的,ALK或ROS1阳性的非小细胞肺癌患者的连续队列。
对于ALK阳性的患者,劳拉替尼治疗开始的中位PFS和OS分别为11.8个月和无法告知,对于ROS1阳性的患者,劳拉替尼治疗开始的中位PFS和OS分别为7.6个月和20.9个月。对于ALK阳性患者,客观缓解率和疾病控制率分别为46.2%和86.2%,对于ROS1阳性的患者,客观缓解率和疾病控制率分别为47.1%和88.2%。中枢神经系统的客观缓解率分别为41.7%和37.7%。中位随访时间为15.6个月, 在劳拉替尼治疗下,观察到50%的ALK阳性患者和61%的ROS1阳性患者出现疾病进展, 分别有34%和23%的患者出现了中枢神经系统进展。
BRIGHTSTAR: 一个布加替尼+局部巩固疗法治疗未使用TKI的ALK重排非小细胞肺癌患者的试验。(摘要号:9624)
BRIGHTSTAR: A pilot trial of local consolidative therapy (LCT) with brigatinib in tyrosine kinase inhibitor (TKI)-nave ALK-rearranged advanced NSCLC.
方法
这是一个单中心的调查员启动的试验,评估布加替尼+局部巩固疗法的安全性,可行性和有效性。符合条件的患者为未使用TKI的ALK重新排列的晚期非小细胞肺癌患者,伴有任何数量的转移。使用布加替尼治疗的患者,诱导期为8周,然后使用放射和/或手术进行局部巩固治疗。
截至2020年2月1日,对16例患者进行了反应评估,并完成了局部巩固治疗,1例患者仍在诱导布加替尼上。疾病控制率为100%,客观反应率为94%。(n = 15).中位随访时间为8个月,到截止日,没有患者出现疾病进展。
3. RET
BLU-667治疗RET融合NSCLC的ARROW1/2期研究的注册数据集(摘要号9515)
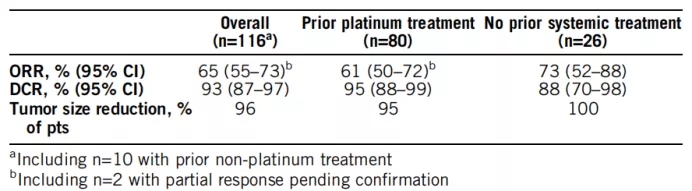
Registrational dataset from the phase I/II ARROW trial of pralsetinib (BLU-667) in patients (pts) with advanced RET fusion+ non-small cell lung cancer (NSCLC).
共纳入116例晚期NSCLC患者,其中26例为初治。总人群ORR为65%,DCR为93%,中位DOR未达到。无论是初治或经治,BLU667都有不错的疗效(ORR为73%,61%)。
LOXO-292治疗RET融合NSCLC的颅内疗效:LIBRETTO-001试验(摘要号9516)
Intracranial activity of selpercatinib (LOXO-292) in RET fusion-positive nonsmall cell lung cancer (NSCLC) patients on the LIBRETTO-001 trial
LOXO-292为高选择性RET抑制剂。在LIBRETTO-001研究中,共纳入了79例RET融合NSCLC患者,其中22例有可测量脑转移病灶,14例可评估颅内疗效。有5例在LOXO-292治疗2个月前做过脑部放疗。14例患者的颅内ORR达到93%之高,包括2例达到了CR。中位颅内DOR为10.1个月。
4. MET
沃利替尼治疗MET14跳跃突变肺肉瘤样癌及其他类型NSCLC的II期研究(摘要号9519)
Phase II study of savolitinib in patients (pts) with pulmonary sarcomatoid carcinoma (PSC) and other types of non-small cell lung cancer (NSCLC) harboring MET exon 14 skipping mutations (METex14+)
陆舜教授领衔开展的一项沃利替尼治疗MET14突变肺癌的多中心II期临床研究结果正式面世。研究纳入了70例MET14突变的非小细胞肺癌患,其中57.1%的患者属于肺腺癌,35.7%的患者属于肺肉瘤样癌(PSC)。分期上,92.9%的患者属于IV期患者,60%的患者属于经治患者。所有患者接受沃利替尼 (600mg (50kg以上);400mg(50kg以下))的治疗。主要研究终点为ORR。研究结果显示,在61例可评价疗效的患者中,整体有效率为47.5%,疾病控制率高达93.4%。中位PFS是6.8个月。
MET/AXL/VEGFR-2抑制剂ningetinib联合吉非替尼治疗中国EGFR-TKI耐药T790M阴性NSCLC(摘要号9583)
A phase Ib study of a novel c-MET, AXL and VEGFR-2 inhibitor ningetinib and gefitinib combination therapy in Chinese EGFR-TKI resistant NSCLC with T790M negative.
这项1b期研究入组了既往EGFR-TKI耐药后T790M阴性的患者,使用ningetinib30-60mg+吉非替尼250mg每日进行治疗。结果显示,纳入的86例患者既往用过EGFR-TKI治疗线数分别为1线66%,2线33%,3线1%。84例可评估患者的ORR为19.1%,DCR为91.7%,中位PFS为4.4个月。在接受过3代EGFR-TKI及脑转移亚组中,PFS无差异。MET高拷贝数患者的疗效更佳,GCN≥6的ORR为36.4%,GCN≥5的ORR为25%,GCN≥3的ORR为21.6%。
Tepotinib治疗MET 14跳跃的生物标志物及疗效分析:VISION研究(摘要号9556)
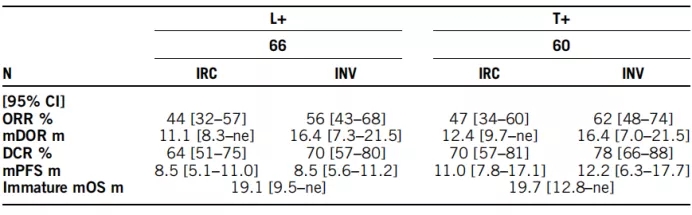
Primary efficacy and biomarker analyses from the VISION study of tepotinib in patients (pts) with non-small cell lung cancer (NSCLC) with METex14 skipping
该药已在日本上市,在VISION研究中纳入了151例MET14+患者使用tepotinib进行治疗,按照MET14检测方式分为三组:L+(液体活检)、T+(组织检测)、L+和/或T+。结果显示,无论是L+或T+,疗效相似。ORR为44%,47%,中位PFS为8.5,11个月。
Capmatinib治疗高水平MET扩增及(或)MET 14突变晚期NSCLC:2期GEOMETRY mono-1研究(摘要号9509,9520)
Capmatinib in patients with high-level MET-amplified advanced non-small cell lung cancer (NSCLC): results from the phase 2 GEOMETRY mono-1 study.
Capmatinib in patients with METex14-mutated or high-level MET-amplified advanced non-small-cell lung cancer (NSCLC): results from cohort 6 of the phase 2 GEOMETRY mono-1 study.
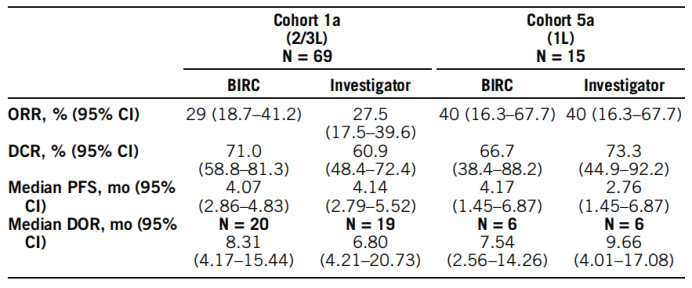
Capmatinib是FDA批准的首个选择性MET抑制剂,既往公布了该药2期研究的队列4(ME14阳性经治)和队列5b(MET14阳性初治)的结果,本次报道了队列1a和队列5a的数据,分别为高水平MET扩增(基因拷贝数≥10)既往接受过1/2线治疗,以及初治的患者。队列1a和5a共纳入了69例和15例患者。Capamatinib后线治疗的ORR为29%,中位DOR为8.31个月,中位PFS为4.17个月;一线治疗的ORR为40%,中位DOR为7.54个月,中位PFS为4.07个月。
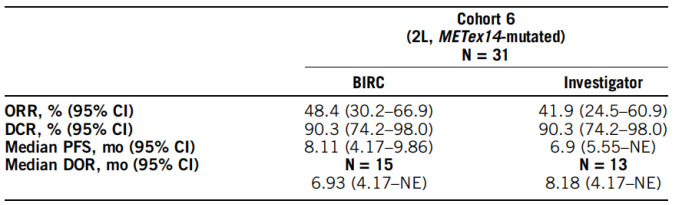
在同一研究的队列6中,纳入了34例MET14突变或高水平MET扩增的NSCLC患者。在MET14+患者中,BIRC评估的ORR为48.4%,中位DOR为6.93个月,中位PFS为8.11个月。3例MET扩增患者都为SD。
MET单抗混合物Sym015治疗MET 14/扩增晚期NSCLC(摘要号9510)
Safety and preliminary clinical activity of the MET antibody mixture, Sym015 in advanced non-small cell lung cancer (NSCLC) patients with MET amplification/exon 14 deletion
Sym015为2个人源化抗体的混合物,对MET下调有超精准的作用。本次大会报道了2a期的研究,纳入了12例MET 14跳跃突变及8例MET扩增的晚期NSCLC患者。结果显示,总人群的ORR为25%,MET14+和扩增组的ORR分别都是25%。DCR为80%,中位PFS为5.5个月。在10例未接受过MET-TKI的患者中,ORR为50%,DCR为100%,PFS为6.5个月。经治患者的DCR为60%,PFS为5.4个月。中位OS未达到。
5. HER2/CEACAM5/其他靶点
DS-8201治疗HER2突变晚期NSCLC:DESTINY-Lung01的中期结果(摘要号9504,口头报道)
Trastuzumab deruxtecan (T-DXd; DS-8201) in patients with HER2-mutated metastatic non-small cell lung cancer (NSCLC): Interim results of DESTINY Lung01.
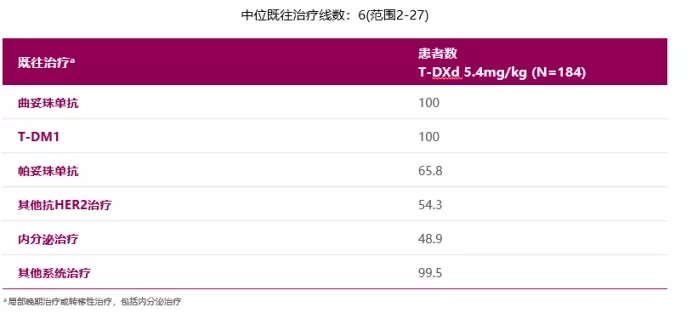
DS-8201为针对HER2靶点的ADC(抗体偶联物)药物,已经获得FDA批准用于乳腺癌。本次ASCO将公布DS-8201在肺癌的初期数据。截至2019.11.25,共纳入了42例HER2过表达或HER2激活突变的晚期NSCLC患者,其中45.2%具有脑转移。患者的既往中位治疗线数为2,90.5%患者既往接受过含铂双药化疗,54.8%患者接受过免疫治疗。中位治疗持续时间为7.75个月。经ICR(独立中心评审)确认的ORR为61.9%,中位DOR未达到,DCR为90.5%,预估的中位PFS为14个月。
ADC药物SAR408701治疗表达CEACAM5的非鳞NSCLC患者(摘要号9505,口头报道)
Efficacy and safety of the antibody-drug conjugate (ADC) SAR408701 in patients (pts) with non-squamous non-small cell lung cancer (NSQ NSCLC) expressing carcinoembryonic antigen-related cell adhesion molecule 5 (CEACAM5).
这项研究纳入了表达CEACAM5(癌胚抗原相关细胞粘附分子5)的晚期非鳞NSCLC患者,CEACAM5在免疫组化的表达≥2+,使用ADC药物SAR408701(100mg/m2,q2w)治疗。结果显示,92例患者中分别有28例和64例为CEACAM5中等和高表达。在中等表达队列,ORR为7.1%,高表达队列的ORR为20.3%,DCR为62.5%。既往接受过PD1/PDL1免疫治疗患者的ORR为17.8%。
TAK228治疗携带NFE2L2和KEAP1基因突变的晚期非小细胞肺癌患者的II阶段研究(摘要号:9607)
Phase II study of TAK228 in patients with advanced non-small cell lung cancer (NSCLC) harboring NFE2L2 and KEAP1 mutations.
用LK-2LUSC,A549 ADCL进行细胞系和异种移植实验 , SK-MES-1 LUSC肺鳞癌细胞(NFE2L2/KEAP1 WT) 用TAK-228, 奥利默斯, 雷帕霉素或去复利莫司治疗。
21个可评价的患者已经被治疗(10 NFE2L2, 6 KEAP1, 5 KRAS+NFE2L2/KEAP1). 中位年龄为70,中位之前的治疗线数为2,吸烟者为100%, 最常见的治疗相关不良反应包括高血糖(72%)、疲劳(32%),腹泻(32%),食欲下降(32%)在NFE2L2 突变的肺鳞癌患者中, 客观缓解率(ORR )为 20% , 疾病控制率(DCR )为 100% ,中位无进展生存期( PFS) 为 8.9个月 (95%CI 7-NR). 在KEAP1突变的肺鳞癌患者组,客观缓解率( ORR) =为17%,疾病控制率( DCR )=为67% ,无进展生存期(PFS)范围 =为1.8-8.6 个月。在 KRAS + NFE2L2/KEAP1 突变患者组, ORR = 0% and DCR = 0%.
二、免疫篇
1.O药+伊匹单抗vs化疗一线治疗晚期NSCLC的:CheckMate227的3年数据更新(摘要号9500,口头报道)
Nivolumab + ipilimumab versus platinum-doublet chemotherapy as first-line treatment for advanced non-small cell lung cancer: Three-year update from CheckMate 227 Part 1
CheckMate227是NSCLC首个双免疫取得阳性结果的III期研究,目前O药+伊匹单抗(CTLA-4抑制剂)也获得了FDA加速批准用于EGFR/ALK阴性NSCLC一线治疗。既往数据显示,无论是PDL1阳性(≥1%)或阴性(<1%),O药3mg/kg(q2w)+伊匹1mg/kg(q6w)的总生存期OS都优于传统化疗。此次ASCO更新3年数据。截止2020年2月28日,中位随访时间为43.1个月。
①PDL1≥1%患者持续从双免疫治疗中得到OS获益(HR=0.79,95%CI 0.67-0.93),3年生存率为33%(O药+伊匹),29%(O药)和22%(化疗),也意味着三分之一患者用双免疫活过了3年,相比下化疗组只有五分之一。
②PDL1≥1%患者在3年时,O药+伊匹组有18%的患者仍然未出现疾病进展,O药组的3年PFS率为12%,化疗组为4%。双免疫将PFS率提高了超过4倍!达到肿瘤缓解的患者中,O药+伊匹组有38%在3年时未出现进展,O药组为32%,而化疗组只有4%。
③PDL1<1%患者中,双免疫的OS也持续获益(HR=0.64,95%CI 0.51-0.81),3年生存率为34%(O药+伊匹)、20%(O药+化疗)和15%(化疗);13%、8%和2%的患者达到持续的3年PFS;分别有34%、15%和0%的肿瘤缓解患者在3年时为出现疾病进展。
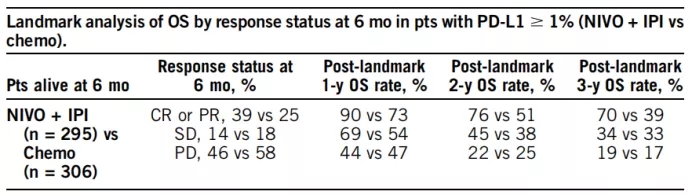
④PDL1≥1%的患者,在6个月时若达到完全缓解CR/部分缓解PR,O药+伊匹组有更长的OS(1年、2年和3年生存率如下表),双免疫的3年生存率可以达到70%之高!
可以看到,无论PDL1是否阳性,双免疫的长期生存情况相似,且获益都优于化疗。
2.O药+伊匹+2周期化疗vs 4周期化疗一线治疗晚期NSCLC:CheckMate9LA(摘要号9501,口头报道)
Nivolumab (NIVO) + ipilimumab (IPI) + 2 cycles of platinum-doublet chemotherapy (chemo) vs 4 cycles chemo as first-line (1L) treatment (tx) for stage IV/recurrent non-small cell lung cancer (NSCLC): CheckMate 9LA.
CheckMate9LA III期研究中纳入EGFR/ALK阴性晚期NSCLC患者,使用O药360mg(q3w)+伊匹1mg/kg(q6w)+化疗(2周期)或单纯4周期化疗治疗,既往BMS官网报道过阳性结果的消息。结果显示,相比单纯化疗,O药+伊匹+化疗组的OS明显延长,为15.6 vs 10.9个月(HR=0.66,P5%CI 0.55-0.80),两组一年生存率为63% vs 47%。联合组的ORR和PFS也得到了获益。在各个亚组中(包括关键的PDL1表达分层和病理类型),获益均可见。
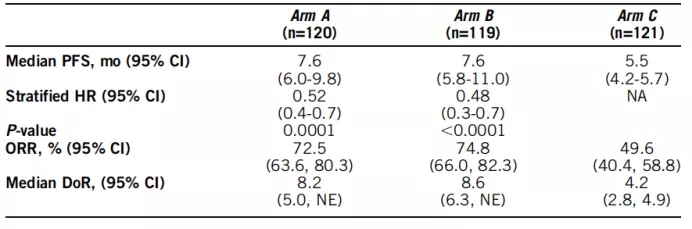
3.替雷利珠单抗+化疗vs化疗一线治疗鳞状NSCLC的III期研究(摘要号9554)
替雷利珠单抗为百济神州研发的国产PD1单抗,目前已经在国内上市,本次大会将公布替雷利珠单抗+化疗一线治疗肺鳞癌的III期研究结果。纳入的360例患者为中国晚期NSCLC患者,分为三组:A组PD1+紫杉醇+卡铂vs B组PD1+白蛋白紫杉醇+卡铂 vs C组紫杉醇+卡铂。结果显示,替雷利珠单抗+化疗(A和B组)的中位PFS明显优于化疗组,为7.6 vs 7.6 vs 5.5个月。HR为0.52和0.48.中位OS均未达到。A B C三组的中位DOR为8.2 vs 8.6 vs 4.2个月。
4.M7824(TGF-β和PDL1双功能融合蛋白)二线治疗NSCLC(摘要号9558)
Two-year follow-up of bintrafusp alfa, a bifunctional fusion protein targeting TGF-b and PD-L1, for second-line (2L) treatment of non-small cell lung cancer (NSCLC)
M7824为TGFβ和PDL1双特异抗体,有着“二代PD1”的特性。这次ASCO公布该药二线治疗NSCLC的I期研究结果。共纳入了40例患者,接受了2期推荐剂量1200mg,q2w治疗。ORR为27.5%,中位DOR为18个月。18个月和24个月的PFS率为18.4%和11%。18个月和24个月OS率为49.7%和39.7%,DOR率分别为42.4%和21.2%。PDL1阳性患者的中位OS达到21.7个月。
5.Durvalumab+Tremelimumab±化疗治疗晚期NSCLC患者:CCTG BR.34(摘要号9502,口头报道)
CCTG BR.34: A randomized trial of Durvalumab and tremelimumab +/- platinum-based chemotherapy in patients with metastatic (Stage IV) squamous or nonsquamous non-small cell lung cancer (NSCLC).
CCTG BR.34研究中,纳入了301例EGFR/ALK阴性晚期NSCLC患者,使用PDL1单抗Durvalumab(度伐利尤单抗)+Tremelimumab(CTLA4抑制剂)+化疗vs Durvalumab+treme进行治疗。结果显示,两组OS没有显著差异,分别为16.6(D+T+化疗) vs 14.1个月(D+T)。D+T+化疗组显著延长了中位PFS(为7.7 vs 3.2个月,HR=0.67,95%CI 0.52-0.88)。根据TMB、性别、年龄或吸烟状态分层,两组结果无差异。在PDL1 TPS≥50%患者中,D+T+化疗组的OS有获益的趋势(HR=0.64,P=0.07)。两组中血浆TMB<20的患者都与生存缩短有关(HR=1.99)。
6.尼达尼布+多西他赛治疗用免疫检查点抑制剂治疗后的肺腺癌患者(摘要号:9604)
这一最新的分析是正在进行的NIS VARGADO研究的一部分 (队列 B),一个对于非小细胞肺腺癌患者一线化疗后用尼达尼布+多西他赛治疗的前瞻性非介入治疗。这个分析包括57名之前既接受了化疗也接受了免疫检查点抑制剂治疗的患者。
在尼达尼布和多西他赛治疗下,客观缓解率(ORR)为50%;疾病控制率(DCR)为85.0%。中位无进展生存期为6.5个月, 中位总生存为12.4个月(95%CI 11.4 – 14.1).
7.SWOG S1400F:德瓦鲁单抗+tremelimumab治疗之前用PD-1检查点抑制剂治疗耐药德IV期肺鳞癌患者德II期研究。(摘要号:9623)
方法: 合格患者为先前治疗过的肺鳞癌患者,表现状态评分为0-1,有合格的器官功能,在24小时的抗PD-1单药治疗后出现了疾病进展。患者接受D1500mg+T75mg静注,每28天一次,持续4个周期,然后用D维持治疗,直到疾病进展。
结果
对先前PD-(L)1治疗的最佳反应为在 3/7/20个患者中,出现了 CR/PR/SD,抗PD-(L)1治疗的中位反应持续时间为8.6个月。D+T没有观察到客观反应; 47%患者为 疾病稳定作为最佳反应 。中位PFS为2个月,幸存实际为7.5个月。在14位疾病稳定作为最佳反应的患者中,中位PFS从第一个疾病评估开始计算为2.8个月。
8.O药+HS-110后线治疗NSCLC(摘要号9546)
Tumor antigen expression and survival of patients with previously treated advanced non-small cell lung cancer (NSCLC) receiving viagenpumatucel-L (HS-110) plus nivolumab.
HS-110是一种同种异体肿瘤细胞疫苗。该研究的队列A纳入了经治的NSCLC患者(未接受过免疫治疗),使用HS-110+O药治疗,结果显示,ORR为21%,临床获益率为43%,中位DOR为17.2个月。中位OS为28.7个月,1年生存率为57%,2年生存率为36%。
9.Tiragolumab+T药vs T药一线治疗PDL1阳性晚期NSCLC的II期随机双盲试验:CITYSCAPE(摘要号9503,口头报道)
Primary analysis of a randomized, double-blind, phase II study of the antiTIGIT antibody tiragolumab (tira) plus atezolizumab (atezo) versus placebo plus atezo as first-line (1L) treatment in patients with PD-L1-selected NSCLC (CITYSCAPE)
Tiragolumab为抗TIGIT单克隆抗体,是新型免疫检查点抑制剂。这项II期随机双盲研究纳入了EGFR/ALK阴性PDL1阳性(TPS≥1%)的晚期NSCLC患者,一线使用Tiragolumab+PDL1单抗T药(阿替利珠单抗)vs T药进行治疗。这项双免疫治疗的试验共纳入135患者。截止2019年12月,联合组的ORR明显优于单药组(37.3% vs 20.6%),中位PFS也获得明显延长,为5.6 vs 3.9个月。下表为2019年6月初期分析时的结果,两组3级及以上TRAE(治疗相关不良反应)发生率为19.1% vs 14.9%。
10.以帕博珠利单抗为基础治疗合并脑转的转移性非小细胞肺癌患者的结果。(摘要号9599)
Outcomes in patients with metastatic non-small cell lung cancer (mNSCLC) with brain metastases treated with pembrolizumab-based therapy.
对转移性非小细胞肺癌患者用帕博珠利单抗+/-化疗治疗进行了一个回顾性的单中心研究。
大部分有活跃脑转移的患者要么在帕博珠利单抗治疗开始之前30天或者在帕博珠利单抗治疗开始之后进行了放射学治疗,在剩余的13个单独使用帕博珠利单抗为基础治疗的患者中,颅内反应包括2例完全缓解,2例部分缓解,3例疾病稳定,和4例疾病进展。截止到2020年1月1日,在15个月的中位随访时间内,在用帕博珠利单抗治疗的患者队列,有或者没有脑转移的患者之间,中位无进展生存期(PFS)没有区别(9.2 vs 7.3 个月, p = 0.41) ,中位总生存(OS)也没有差别 (18.3 vs 18.0 个月, p = 0.67) . 在多变量分析中,女性性别、ECOG 0-1、腺癌组织学和帕博珠利单抗作为一线治疗与改善PFS和OS有关。
11.Abemaciclib+K药治疗肺鳞癌,以及KRAS突变非鳞NSCLC的1b期研究(摘要号9562)
A phase Ib study of abemaciclib in combination with pembrolizumab for patients (pts) with stage IV Kirsten rat sarcoma mutant (KRAS-mut) or squamous non-small cell lung cancer (NSCLC) (NCT02779751): Interim results.
Abemaciclib是一款CDK4/6抑制剂的口服药物。这项1b期研究的队列A纳入了为接受过化疗的KRAS阳性PDL1阳性(≥1%)非鳞癌,队列B纳入既往接受过≤1线铂类化疗晚期NSCLC。两个队列个入组了25例患者。队列A患者的ORR为24%,队列B为8%。两组的DCR为52%和64%。总体疗效一般,与K药单药间接相比为展现明显的优势。
12.卡博替尼联合T药治疗先前用免疫检查点抑制剂治疗过的非小细胞肺癌患者:来自COSMIC-021研究队列7的结果(摘要号:9610)
Cabozantinib in combination with atezolizumab in non-small cell lung cancer (NSCLC) patients previously treated with an immune checkpoint inhibitor: Results from cohort 7 of the COSMIC-021 study.
方法
患者接受了卡博替尼40mg,口服,每日一次和T药1200mg静注,每三周一次的治疗
结果
30例晚期非小细胞肺癌患者参与了研究。截止到2019年12月20日,中位随访时间为8.9个月,9位患者持续研究治疗。确认的客观缓解率( ORR )为 23%。反应时间为1.4 个月 , 中位的反应持续时间为 5.6 个月. 疾病控制率(DCR )为 83%.
小细胞肺癌
1. Durvalumab+化疗一线治疗SCLC的脑转移效果(摘要号9068)
CASPIAN研究为Durvalumab+化疗vs化疗一线治疗SCLC的研究。此次报道了脑转移的亚组数据。基线时,D+化疗组和化疗组的脑转移比例为10.4%和10%。无论有无脑转,D+化疗都改善了PFS(有脑转HR0.73,无脑转0.78)和OS(有脑转HR0.69,无脑转0.74)。在基线无脑转移的患者中,D+化疗组和化疗组新出现脑转移的发生率为8.3% vs 9.5%。Durvalumab+化疗对SCLC脑转移患者展现了客观的疗效。
2. 安罗替尼+化疗一线治疗广泛期SCLC的II期研究(摘要号9066)
纳入了国内27例SCLC患者,安罗替尼+化疗一线治疗的ORR竟然达到77.78%之高,中位PFS为9.6个月,DCR为96.3%。从数据来看,该组合的疗效已经超过了现有的SCLC一线治疗效果,可期。
3. Cediranib+奥拉帕利治疗铂类进展的SCLC患者的II期研究(摘要号9065)
Cediranib为泛VEGFR-TKI。这项II期研究使用该药联合奥拉帕利进行治疗。25例患者中,有52%既往用过免疫治疗,结果显示ORR为28%,中位DOR为3.8个月,DCR为88%。
4. 化疗±O药作为广泛期小细胞肺癌的前线治疗的随机II期临床试验:ECOG-ACRINEA5161。(摘要号9000)
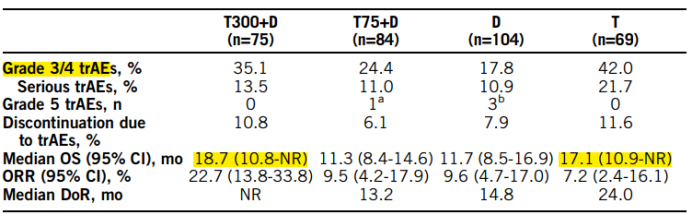
可测量的广泛期小细胞肺癌患者,ECOG评分为0或1,还未接受对于广泛期小细胞肺癌的全身治疗的患者参与了研究。将病人随机1:1分配到O药360mg+CE每21天,持续4个周期,接着用O药240mg每2个星期维持治疗,直到疾病进展,或到2年(组A),或CE每21天持续4个周期,接着观察(组B)。
这项研究2018年5月启动,2018年12月完全获利。160 个患者参与. 在ITT人群中,O药+CE相比CE明显改善了PFS,中位PFS分别为5.5对比4.6个月。 次要的O药+CE的OS的终点对比CE也改善了,中位OS为11.3对比8.5个月。在开始研究治疗的患者中,O药+CE相比 CE明显改善了PFS,中位PFS分别为5.5对比4.7个月;在这组人群中,O药+CE对比CE,OS也改善了,中位OS为11.3个月对比9.3个月。ORR为52.29%对比47.71%。
肝胆肿瘤
本次ASCO肝胆肿瘤有3项研究荣登ASCO口头报道,分别为多纳非尼,阿帕替尼以及PD-L1单抗Durvalumab联合CTLA-4单抗tremelizumab的黄金组合。
1、国产靶向新药多纳非尼:高效低毒优于索拉非尼
摘要号:4506
标题:多纳非尼对比索拉非尼一线治疗晚期肝细胞癌的开放标签,随机,多中心II / III期试验(ZGDH3)。
该试验共纳入668例既往未接受过全身化疗和/或分子靶向治疗的不可手术或转移性肝细胞癌患者,按照1:1的比例随机分成多纳非尼组(200mg,一天两次)和索拉菲尼组(400mg,一天两次)。该试验的主要研究终点为总生存时间(OS)。次要研究终点无进展生存时间(PFS)、肿瘤进展时间(TTP)、客观缓解率(ORR)和疾病控制率(DCR)、安全性等。
试验结果(多纳非尼VS 索拉非尼):
1、 mOS:12.1个月vs 10.3个月(危险比为0.831,95%置信区间0.699– 0.988,p = 0.0363)
2、 ITT(意图治疗):12.0个月vs 10.1个月(危险比为0.839, 95%置 信区间0.706–0.996, p = 0.0446)
3、 mPFS:3.7个月vs 3.6个月(p = 0.2824),差别不大
4、 ORR:4.6% vs 2.7%(p =0.2448)
5、 DCR:30.8% vs 28.7%(p = 0.5532)
6、 ≥3级不良反应:57.4% vs 67.5%(p = 0.0082),多纳非尼严重不良事件报告患者数量较少(16.5% vs 20.2%,p = 0.2307)。
多纳非尼的常见不良反应:手足皮肤反应(50.5%),天冬氨酸转氨酶升高(40.5%), 血胆红素增加(39.0%),血小板计数减少(37.8%),以及 腹泻(36.6%)。
多纳非尼是中国十年来首次在ASCO大会上向全世界公布创新药物一线治疗晚期肝细胞癌的大型临床研究成果和数据,其低毒高效的特性相信会为给更多肝癌患者带来长生存的希望。
2、国产靶向新药阿帕替尼:二线单药治疗mOS达8.7个月
摘要号:4507
标题:AHELP研究:阿帕替尼二线治疗中国晚期肝癌患者:一项随机、安慰剂对照、双盲III期研究
AHELP研究旨在观察和评价阿帕替尼二线治疗晚期HCC患者的有效性和安全性。共纳入了393例既往接受过至少一线系统性治疗后失败或不可耐受的晚期HCC患者,随机分配:
阿帕替尼试验组(n=261、口服,750mg/天,28天一疗程)
安慰剂对照组(n=132,每天口服,28天一疗程)。
主要研究终点为总生存期(OS),次要研究终点包括无进展生存期(PFS)、疾病进展时间(TTP)、客观缓解率(ORR)、缓解持续时间(DoR)、疾病控制率(DCR)和安全性等指标。
试验结果(阿帕替尼VS安慰剂):
1、 mOS:8.7个月[95%可信区间7.5-9.8] vs 6.8个月[95%可信区间5.7-9.1](危险比0.785 [95%置信区间0.617-0.998];p=0.0476)
2、 PFS:4.5个月[95% CI 3.9-4.7] vs 1.9 个月[95% CI 1.9-2.0](危险比0.471 [95% CI 0.369-0.601]; p˂0.0001)
3、 ORR:10.7% (95% CI 7.2-15.1) vs 1.5% (95% CI 0.2-5.4)
4、 治疗相关不良事件(TRAEs):97.3% vs 70.8%,
阿帕替尼三、四级常见不良反应:高血压(27.6%),手足综合征(17.9%),血小板减少(13.2%),中性粒细胞减少(10.5%)。
阿帕替尼的mOS与老牌二线雷莫卢单抗(mOS:8.5个月)的试验结果相当,作为国产药物更期待价格上能惠及患者。
3、双免黄金搭档:D+T治疗晚期HCC,mOS达18.7m
摘要号:4508
标题:PD-L1单抗Durvaluamb(德瓦鲁单抗,D药)联合CTLA-4单抗tremelimumab(T药)治疗晚期肝细胞癌的疗效、耐受性和生物学活性
该试验共纳入332名患者,分为四组:
1、 T300+D组:患者使用300 mg T药+ 1500 mg D药 1个疗程后使用D药 [Q4W]
2、 T75+D组:患者使用75mg T药+ 1500 mg D药4个疗程后使用D药 [Q4W]
3、 单药D组:患者使用1500 mg(Q4W)
4、 单药T组:患者使用750 mg(Q4W).
该试验的主要研究终点是安全性。次要研究终点ORR、反应持续时间(DoR)、循环淋巴细胞和总生存率(OS)。
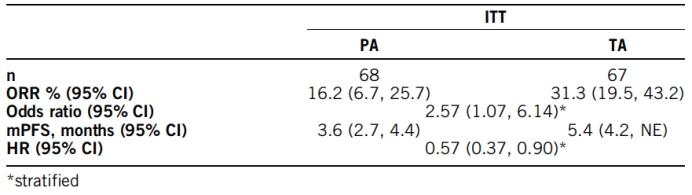
试验结果(T300+D组VS T75+D组VS单药D组VS单药T组)
1、 mOS:18.7 (10.8-NR)vs11.3 (8.4-14.6) 11.7 (8.5-16.9) 17.1个月(10.9-NR)
2、 ORR:22.7% (13.8-33.8) vs 9.5% (4.2-17.9) vs 9.6%(4.7-17.0) vs 7.2%(2.4-16.1)
3、 3/4级不良反应:35.1%vs 24.4%vs 17.8%vs 42.0%
我们不难看出与T75+D或单一疗法相比,T300+D方案无论是从mOS还是ORR,都进一步支持了其在晚期肝细胞癌(aHCC)上的显著疗效。正在进行的HIMALAYA III期研究正在评估T300+D和D对索拉非尼一线治疗HCC的疗效(NCT03298451)。
摘要号:4519,壁报号127
标题:PD-1单抗keytruda联合仑伐替尼一线治疗晚期不可手术的肝细胞癌的疗效、耐受性和生物学活性的Ib期研究
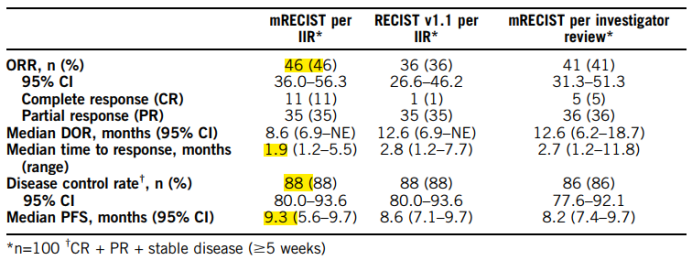
试验结果(根据mRECIST评估):
1、 ORR:46%,其中CR达11%
2、 DCR:88%
3、 中位DOR:8.6个月(95%CI,6.9-NE)
4、 mPFS:9.3个月。
此外最新一期NEJM公布了PD-L1抑制剂阿替利珠单抗(Atezolizumab)联合抗血管生成药贝伐珠单抗(Bevacizumab)用于治疗既往未接受过系统性治疗的不可切除的肝细胞癌(HCC)患者的临床III期试验——IMbrave150的完整数据:T+A方案使患者一年生存率提高至67.2%!免疫靶向的组合方案真是在肝癌领域怕频频给大家带来惊喜,也希望听到更多的阳性结果!
摘要号:e16602
标题:肝动脉灌注化疗联合阿帕替尼和特瑞普利单抗治疗晚期肝细胞癌:来自单中心的真实世界数据
2019年4月-8月,纳入6例晚期HCC患者,所有患者均接受了6个周期HAIC(序贯给予奥沙利铂,亚叶酸,氟尿嘧啶)。
试验结果:
1、 PR:按照RECIST评估,6例均为PR;而按照mRECIST评估,则3例CR和3例PR
2、 中位至缓解时间:1.3个月(0.7-2.0)
3、 血液中的生物标记物:logAFP基线: 3.2±1.6, 末次随访: 1.3±1.4; p = 0.029和logPIVKA-II基线: 4.4±0.6, 末次随访: 2.0±1.4; p = 0.006均在治疗后显著降低。
4、 最常见的不良事件:高血压、手足综合征以及厌食症,在所有患者中均观察到。无4/5级不良事件出现。
拓益在肝癌领域荣登ASCO的第二项研究如下:
摘要号:TPS4658 壁报号:266
6、国产安罗替尼联合Penpulimab,DCR达84%
摘要:4592,壁报:200
题目:安罗替尼联合Penpulimab(抗PD-1单抗,AK105)一线治疗晚期肝细胞癌的临床疗效和安全性
试验结果:
1、 ORR:24% (6/25)
2、 DCR:84% (21/25)
3、 TRAEs:93.5%,3级的不良反应发生率在9.7%,无4级的不良反应,最常见的不良反应是谷草转氨酶升高(35.5%)、谷丙转氨酶升高(29%)、乏力(22.6%)、血小板计数降低(19.4%)、血胆红素升高(19.4%), 结合胆红素增加(19.4%)和皮疹(16.1%)。
Penpulimab(AK105)是由康方生物研发的一款国产抗PD-1单抗,安罗替尼是正大天晴研发的多靶点抗血管口服药。期待penpulimab联合安罗替尼(10mg,QD)在HCC一线正在进行的III研究结果。
7、O药联合Y90治疗晚期HCC,中位OS达15.1个月
摘要:4590,壁报号198
摘要号:4601,壁报号209
9、D±T+化疗一线治疗BTC肿瘤,mOS达20.7个月
摘要号:4520,壁报号128
标题:PD-L1单抗Durvaluamb(德瓦鲁单抗)±CTLA-4单抗tremelimumab联合吉西他滨/顺铂(GC)一线治疗晚期胆管癌的疗效、耐受性和生物标记物的II期研究
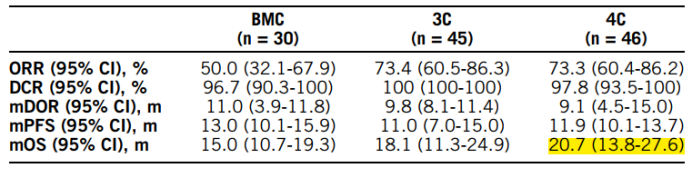
该试验共纳入121名受试者,被分到三个组中:
1、 BMC组(n=30):在第一天和第八天患者接受1个周期的吉西他滨1000 mg/m2 +顺铂25 mg/m2,然后GC联合D药(1120 mg,Q3W)和T药(75 mg,Q3W),
2、 3C(n=45):GC + D药
3、 4C(n=46):GC + D药+T药
试验结果:
1、 mOS :15.0 (10.7-19.3)、18.1 (11.3-24.9)和20.7 (13.8-27.6)个月
2、 ORR:BMC组、3C 组和4C组分别为50.0%(32.1-67.9)、73.4%(60.5-86.3)和73.3%(60.4-86.2)
3、 DCR:BMC组、3C 组和4C组分别为96.7%(90.3-100)、100%(100-100)和97.8%(93.5-100)
4、 不良事件:最常见的是中性粒细胞减少(54.5%)、恶心(59.5%)和瘙痒(55.44%)。最常见的3/4级不良事件是中性粒细胞减少(50.4%), 贫血(35.5%)和血小板减少症(16.5%)。
我司也有幸接到了Durvaluamb相关的肝胆肿瘤相关试验,有兴趣的朋友可以点击原文报名
10、O药联合化疗或者Y药一线治疗晚期不可切除性胆道癌患者的多中心随机II期研究
摘要:4582,壁报号190
题目:PD-1单抗opdivo(O药)联合吉西他滨/顺铂或CTLA-4抑制剂伊匹单抗(ipilimumab,Y药)一线治疗晚期不可切除性胆道癌患者的多中心随机II期研究(BilT-01)。
该实验纳入39例转移性BTCs(胆道肿瘤)患者,其中33名(85%)曾接受过系统治疗(0-2线)。所有患者都接受O药(3mg/kg)和Y药(1mg/kg)治疗,每3周一次,共4次,之后接受O药(3mg/kg)每2周一次。治疗持续长达96周。
主要终点为临床受益率(CBR = CR +PR + SD)。探索终点包括疗效与包括PD-L1表达和肿瘤突变负担在内的生物标志物的相关性。
试验结果:
1、 ORR:24%
2、 CBR:45%。
3、 mOS:6.1个月
4、 mPFS:3.1个月
5、 不良反应
22名(56%)患者出现免疫相关不良事件(irAE),其中8名(20%)患者出现3/4级不良事件。
研究表明,O+Y联合免疫治疗对进展期微卫星稳定型BTC患者具有重要的临床意义,与单药抗pd -1治疗的临床试验相比,应答率较好。
胃肠癌
1.信迪利单抗治疗化疗无效的晚期食道鳞状细胞癌:随机、开放标签II期试验(ORIENT-2)。摘要号:4511
本研究共入组190例受试者,按照1:1随机入组,分别接受达伯舒®(信迪利单抗注射液)或研究者在紫杉醇或伊立替康中选择的治疗药物进行治疗,主要终点是总生存期(OS),探索性研究终点为 PD-L1和NLR对疗效的影响。
1)中位OS:信迪利单抗组明显高于化疗组(7.2m vs. 6.2m,危险[HR] 0.70,P = 0.034)。在信迪利单抗组中,低NLR(<3)的患者的中位OS(HR 0.54,P = 0.019)比高NLR显著更长。
2)ORR:与化疗相比,信迪利单抗的客观缓解率(ORR)更高,分别为12.6%和6.3%,其中PD-L1≥1%的患者,信迪利单抗 vs 化疗为20.2%对0%,针优于化疗,对PD-L1≥10%的患者,信迪利单抗 vs 化疗为35.7%对0%。
3)中位缓解持续时间DOR更长,信迪利单抗 vs 化疗为8.3m vs 6.2m。
2.DS-8201治疗HER2阳性的晚期胃或食管胃交界处(GEJ)腺癌患者:一项随机、II期、多中心、开放标签研究(DESTINY-Gastric01)。摘要号:4513
在TDXd(5.4或6.4 mg / kg)的1期试验中,晚期HER2 +胃癌患者的客观缓解率(ORR)为43.2%(19/44),中位无进展生存期(mPFS)为5.6 个月。
DESTINY-Gastric01研究采用开放标签设计,在日本和韩国的多个中心入组了187例既往接受过2种以上疗法(包括曲妥珠单抗和化疗)的不可手术切除或转移性HER2阳性胃癌或胃食管连接部癌患者,其中日本患者79.7%,韩国患者20.3%。先前接受治疗线程中位值2,近1半先前接受治疗≥3。患者按照2:1随机分组,分别给予DS-8201(6.4mg/kg,每3周1次,n=125)或临床医师选择的化疗(紫杉醇或伊立替康单药,n=62)。
结果:
1)主要终点ORR为 51.3% vs 14.3% (p<0.0001) ,其中11 例患者CR和50例患者PR。确认ORR为42.9%和12.5% (p<0.0001)
2)次要终点:
疾病控制率 DCR ,DS-8201 vs 化疗85.7% vs 14.3%(p=0.0005)
中位持续时间mDOR:DS-8201 vs 化疗为11.3 vs 3.9 m
中位PFS:DS-8201 vs 化疗为5.6 vs 3.5 m (HR, 0.47 ; P = .0003)
mOS :DS-8201 vs 化疗为12.5 vs 8.4 m; HR, 0.59 ; P = .0097
DS8201降低了41%的死亡风险,显著延长OS(先前预设值P = .0202),1年OS 率为52.1% vs 28.9%
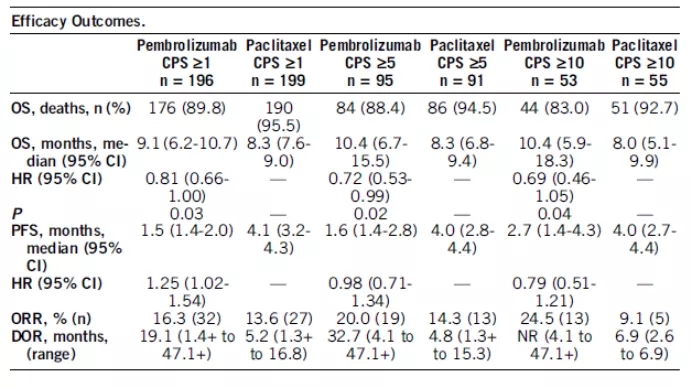
3.Pembrolizumab与紫杉醇用于先前治疗的PD-L1阳性的晚期胃或胃食管交界癌(GC)患者:III期KEYNOTE-061 试验更新。摘要号:4503
KEYNOTE-061研究是一项比较了K药对比紫杉醇治疗铂类和氟尿嘧啶一线化疗后进展的晚期胃癌或胃食管结合部癌患者疗效的全球3期研究。pembrolizumabvs紫杉醇作为GC的二线治疗的全球3期研究。在初步分析(数据截止日期:2017年10月26日)时,针对PD-L1阳性(≥1%)患者,K药与紫杉醇相比没有显着延长总生存期(OS)(9.1mvs 8.3m),但确实引起了更长的反应持续时间(DOR)及更好的安全性。本次ASCO汇报了2年的随访数据(截止日期:2019年10月7日)。
结果:
1.在PD-L1阳性患者中,对比紫杉醇,K药延长了OS,但PFS组之间无明显差异。
2.针对PD-L1≥10%,K药组的ORR较高,DOR则更长。
3.在整个人群中,K药的药物相关不良事件(AEs)少于紫杉醇(53%比84%)。
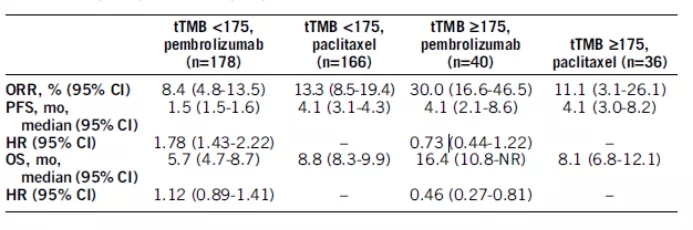
进一步分析发现tTMB的表达高低与K药的疗效成正相关( P<0.001 ),与化疗组的无效没有显著性关系(p>0.600)。在K药和化疗组中,tTMB和PD-L1 表达之间的相关性较低(r<0.18)。
4.康奈非尼(encorafenib)加西妥昔单抗(cetuximab)联合或不联合比美替尼(binimetinib)治疗BRAF V600E转移性结直肠癌与伊立替康或FOLFIRI联合西妥昔单抗的疗效对比:一项随机、三组、III期研究。摘要号4001
本次研究纳入665例BRAF V600E的转移性结直肠癌患者。其中BEACON CRC研究评估了encorafenib(ENCO)+Binimetinb(BINI)+cetuximab(CETUX)的三联方案(n=224)和ENCO加CETUX的二联方案(n=220)与对照组伊立替康+CETUX或FOLFIRI加CETUX(n=221)的疗法对比。
结果(三联组vs二联组vs对照组):
1)mOS:9.3个月(95%置信区间[CI]:8.2,10.8) vs 5.9个月(95%CI:5.1-7.1)(危险比[HR](95%CI)vs 0.60个月(0.47- 0.75)
2)ORR:26.8%(95%CI:21.1%-33.1%) vs 19.5%(95%CI:14.5%-25.4%) vs 1.8%(95%CI:0.5%-4.6%)
3)三联方案和二联方案均表现出更好的OS,从一部分亚组分析表明,一些患者使用三联方案可能受益更多。
试验纳入了42例(21例女性[50%],中位年龄:57.5岁[范围:33-82])的KRAS G12C突变的结直肠癌患者。
结果:
1)13例(31.0%)患者死亡,8例(42.9%)患者仍在治疗中;
2)用药超过3个月的患者22例(52.4%),用药超过6个月的患者8例(19.0%),疾病进展是停药的最常见原因
3)治疗相关不良事件(TRAEs)总20例(47.6%):18例(42.9%)有2级或更低的TRAEs;2例(4.8%)有3级TRAEs,分别为腹泻(2.4%)和贫血(2.4%)。
4)ORR和DCR分别为7.1%(3/42)和76.2%(32/42)。在960mg时,ORR和DCR分别为12.0%(3/25)和80.0%(20/25)。
5)3例PR患者的反应持续时间分别为1.5、4.2和4.3个月,他们的反应仍在数据截止时进行。
6.regorafenib(R)联合avelumab(A)治疗实体瘤的Ⅱ期研究非MSI-H转移性结直肠癌(mCRC)队列的结果。摘要号:4019
这是一项单臂、开放式、多中心的II期试验,评估R(160mgQD3weks/4)+A(每2周 10mg/kg)联合治疗非MSI-HMRC患者(PTS)的疗效和安全性。试验共纳入48例非MSI-H的转移性结直肠癌患者。
1)在40例以影像学资料评估的患者中,有12名(30%)的肿瘤负荷减轻了。
2)病情稳定的患者23例(57.5%)和疾病进展的患者17例(42.5%)。PFS和OS的中位数分别为3.6个月(CI95%:[1.8-5.4])和10.8个月(CI95%:[5.9-NA])。
3)R + A组合达到了PFS和OS,与单独使用R的历史数据相比具有优势。
试验共入组52例顽固性mCRC患者,所有患者接受呋喹替尼(3mg,每日1次,用3周停1周)+信迪利单抗(每次200mg,每3周1次)治疗。
结果:
1)ORR:15.38%(8/52)
2)DCR:57.6%(30/52)
3)mPFS:108天
在发生以下突变的患者中,PFS显著变差:AMER1 (p=0.0073)、DNMT3A (p=0.0075)、ETV5 (p=0.012)、EWSR1 (p=0.016)、FANCA (p=0.019)、IKBKE (p=0.0073)、NOTCH1 (p=0.015)、STAG2 (p=0.012)和TCF7L2 (p=0.0073)。复杂性、凝血级联异常(p = 0.026)、胰腺癌通路异常(p = 0.0098)患者的PFS同样显著变差。
8.Nivolumab (NIVO) +低剂量ipilimumab (IPI)一线治疗微卫星不稳定性高/错配修复缺陷(MSI-H/dMMR)转移性结直肠癌(mCRC):两年临床更新。摘要号:4040
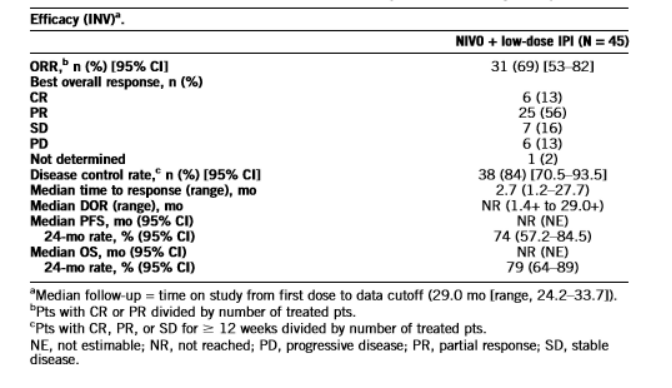
CheckMate 142是一项II期研究,患有MSI-H/dMMR mCRC且未接受转移性疾病治疗的患者(pts)接受NIVO(3 mg/kg Q2W)+低剂量IPI(1 mg/kg Q6W)直至疾病进展或停药。研究主要观察终点为客观反应率(ORR)。
结果:
1)ORR:69%(95% CI 53%~82%),CR 13%
2)mDOR:NR (95% CI 1.4+ to 29.0+)
3)mPFS:NR(NE),24个月PFS率为74% (95% CI 57.2–84.5)
4)mOS:NR(NE),24个月OS率为79% (95% CI 64–89)
1.TAPUR研究:具有BRCA1 / 2失活突变的胰腺癌患者使用Olaparib疗效可观。摘要号:4637
该研究纳入30名患有BRCA1 / 2失活突变的胰腺癌患者,其中有20例先前曾用铂类疗法治疗。这些患者接受奥拉帕利片剂(300mg,n=27)或者胶囊治疗(400mg,n=3)
DCR为31%(90%CI:18%-40%),ORR为4%(95%CI:0%-18%)。7名患者至少有一种3级AE或SAE,至少可能与奥拉帕利有关,包括贫血,腹泻,发烧,肝酶升高,小肠结肠炎,胆红素升高和口腔粘膜炎。
单一疗法在胰腺癌严重预后的种系(OR或SD16 +的5/12 pt)或体细胞(OR或SD16 +的3/16 pt)的BRCA1 / 2失活突变中表现出抗肿瘤活性,扩展了奥拉帕利近期在晚期胰腺癌患者中的研究。
2.Cobimetinib联合吉西他滨治疗KRAS G12R突变的经治的胰腺疾病患者疗效不错。摘要号:4642
胰腺癌患者 KRAS突变的频率为G12D(40%),G12V(30%)和G12R(15-20%),在我们的单组研究中,有13名KRAS突变的胰腺患者(KRAS G12D,G12V和G12R)接受Cobimetinib联合吉西他滨,3周然后休息一周。
结果:
第1组由KRAS G12D / G12V突变的7位患者组成,第2组包括6位KRAS G12R突变的患者。在第1组中,有7名接受治疗的患者在研究中进展并在两个月内死亡。在第2组中,一例患者PR,其他人则疾病稳定SD。中位无进展生存期为6.0个月(95%CI为3-9.3个月),中位OS尚未达到。所有患者均存活8个月。
1、DS-8201,HER2今年最闪耀的星
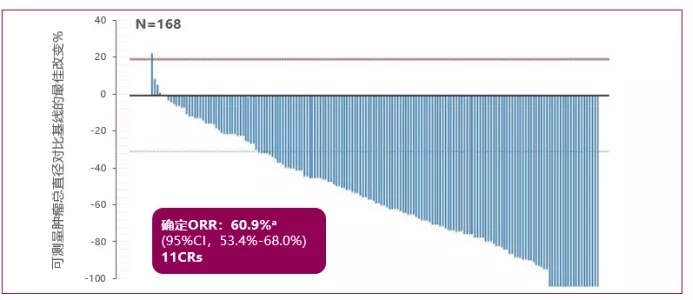
今年一大看点就是HER2新型药物DS-8201的DESTINY-Breast01研究,采用DS-8201后线治疗晚期HER2阳性晚期乳癌患者,有效率高达60.9%!创史上之最。
HER2阳性乳癌类型占比20%左右,目前临床上虽有多种HER2药物可用,但对于多线治疗耐药的后线患者的可用药物少之又少,疗效不理想。DS-8201是一种HER2靶向与化疗偶联的ADC型药物,药理作用优于T-DM1(高细胞膜穿透性及连接物优化),在临床研究中表现出强劲的后线挽救能力。在纳入的中位线数位6线,赫赛汀和T-DM1均需耐药的重度治疗的HER2阳性乳癌耐药后,接受DS-8201治疗,可以获得60.9%的有效率!很难被挑战的数据!
而该药本期的看点不仅在乳癌,还有胃癌数据、结直肠癌数据、肺癌数据、胆管癌数据均会公布。同时,还有与K药联合重磅的研究在开展。已于今年2月份开始招募患者。双枪联合,是否创造奇迹,让人期待!
2、K药挑战三阴乳癌,挫败中靠预测指标挽救,可惜!
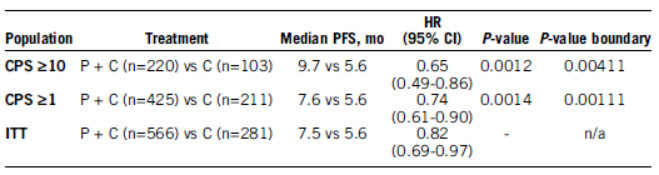
晚期乳癌的首个研究就是KEYNOTE355研究结果呈现,K药+化疗挑战晚期三阴乳癌一线,整体人群中未见统计学差异,但是PDL1≥10%患者产生PFS差异。另一研究提示TMB预测作用。
鉴于T药在三阴乳癌的成功,K药也开启在晚期三阴乳癌的一线研究,入组了未经治疗的局晚或转移性三阴乳癌患者,以2:1的比例随机分组至K药+化疗组或单纯化疗组。PFS为主要研究终点。结果显示,在PDL1≥10%的患者组,K药+化疗组较单纯化疗组,PFS显著提升,分别为9.7:5.6个月,P=0.0012,具有统计学差异。未达到全人群的统计学差异,稍感遗憾。
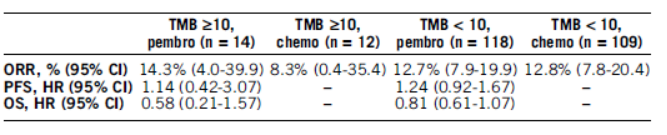
在本次K药在三阴乳癌的另一项临床研究KEYNOTE119研究显示,TMB是预测K药+化疗在三阴乳癌优势人群的指标,TMB≥10的患者组,K药+化疗的疗效明显优于K药组。但TMB<10的患者组,K+化疗与单纯化疗疗效无差异。
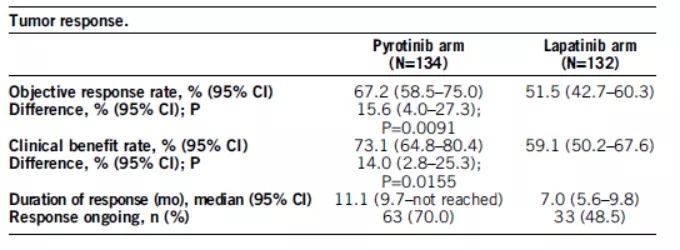
吡咯替尼是国产研发的HER2的小分子药物,III期PHOEBE研究探讨了包含赫赛汀方案在内的方案耐药后的晚期乳癌患者,分别接受吡咯替尼+卡培他滨治疗或传统标准拉帕替尼+卡培他滨治疗。结果显示,主要研究终点PFS,吡咯替尼组明显高于拉帕替尼组,分别为12.5个月:6.8个月[95% CI 0.27–0.56]; P,0.0001)。在赫赛汀耐药的患者中,吡咯替尼组PFS也明显优越,12.5:6.9个月。有效率分别为67.2%:51.5%。最常见的3级以上不良反应是腹泻(30.6%:8.3%)和手足综合征(16.4%:15.2%)。该试验的披露,将动摇拉帕替尼的二线治疗地位,吡咯替尼以全新的疗效优势更替,但不良反应方面需要控制。
4、出现一个强势脑转移控制药物方案,tucatinib
Tucatinib是一种小分子的HER2抑制剂,HER2CLIMB研究纳入了经治的脑转移HER2+晚期乳癌患者,以2:1的比例随机分组至tucatinibb+赫赛汀+卡培他滨组或单纯的赫赛汀+卡培他滨组。结果显示,ORR上,tucatinib组翻倍,47.3%:20%。中枢病灶的PFS上,两组分别为9.9:4.2个月,下降了68%的中枢进展风险。在OS上,两组分别为18.1:12个月,下降了42%的死亡风险。该研究证实了tucatinib的加入,能为晚期重度治疗的脑转移的HER2阳性乳癌患者带来更高的中枢控制疗效和总生存,意义非凡。
扫描上面二维码在移动端打开阅读