免疫细胞疗法治疗人类疾病
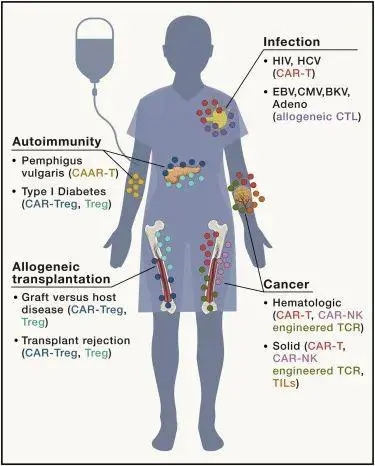
免疫细胞疗法的适用范围逐步扩大,包括癌症,感染,同种异体移植和自身免疫。CAR-T或NK细胞,工程改造的TCR和TIL疗法已经并且正在继续在血液和实体瘤中进行测试。
正在开发Treg,CAR-Treg和CAAR-T细胞,以治疗各种自身免疫性疾病并防止移植组织的排斥。
免疫细胞疗法
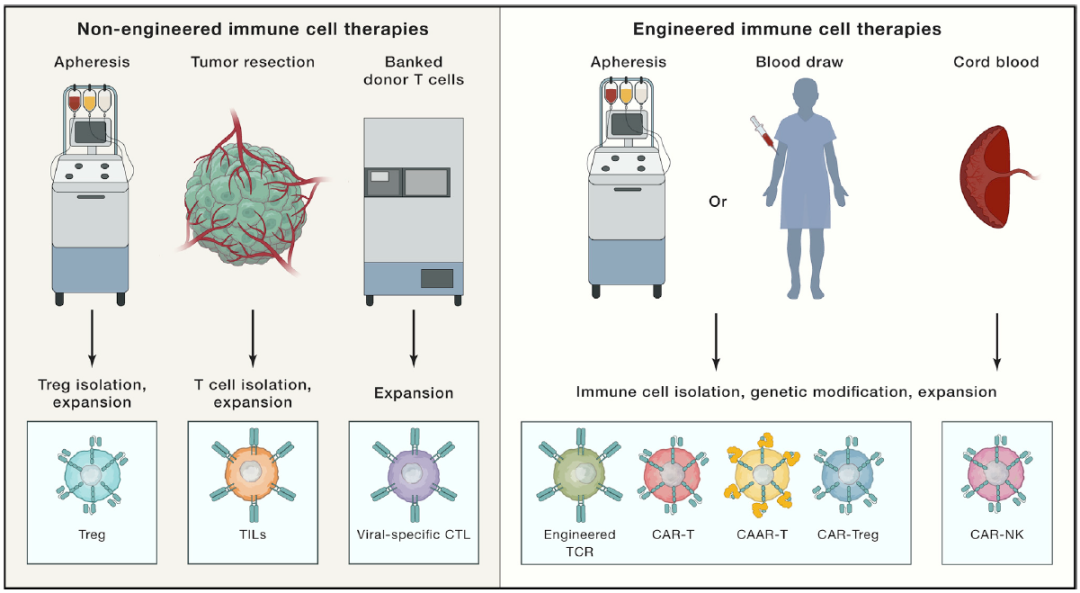
非工程免疫细胞疗法,包括从患者外周血分离的Treg扩增后并回输治疗自身免疫性疾病或GVHD等。从肿瘤(通常是黑色素瘤患者)中分离出肿瘤浸润淋巴细胞(TIL),并扩增回输体内治疗疾病。将病毒特异的CTL复苏,扩增重新输入HLA配型后的患者体内,以治疗慢性感染。
工程免疫细胞疗法,通过自体血液,分离T细胞并使用病毒或非病毒方法进行转基因,构建可以产生工程免疫细胞疗法。
工程T细胞的实例包括:
1)TCR-T细胞;
2)CAR-T细胞或CAR-NK;
3)CAAR-T;
4)CAR-Treg。
02 TIL细胞疗法与CTL细胞疗法
二十世纪八九十年,通过输注经体外扩增的TIL细胞,外加IL-2,能够使得转移性恶性黑色素瘤患者缓解,具有开创性的意义。
尽管TIL疗法在总体临床效应非常有限,一部分是因为从非黑色素瘤患者体内产生的生物活性的TIL不充足。但在个别转移性结直肠癌或乳腺癌治疗中,通过输注TIL后,效果令人惊喜。
20世纪90年代,研究者观察到,接受异体造血干细胞移植后出现复发的患者在输注来自供体的T细胞后,疾病会得到缓解。在患有严重免疫抑制的患者中,异体CTL会诱发机体对EB病毒感染及相关淋巴瘤产生反应,尽管MHC匹配过。
CTL已经可以用来治疗多种病毒感染了。研究人员利用病毒特异性的CTL 来治疗病毒相关癌症前景一片光明,比如EBV、乙肝病毒和其它病毒感染等。
由于病毒相关癌症患者仍会排异异体细胞,研究人员还要关注,采用过继性转移的异体病毒特异性CTL 或TCR-T细胞。
03 工程免疫细胞疗法开发
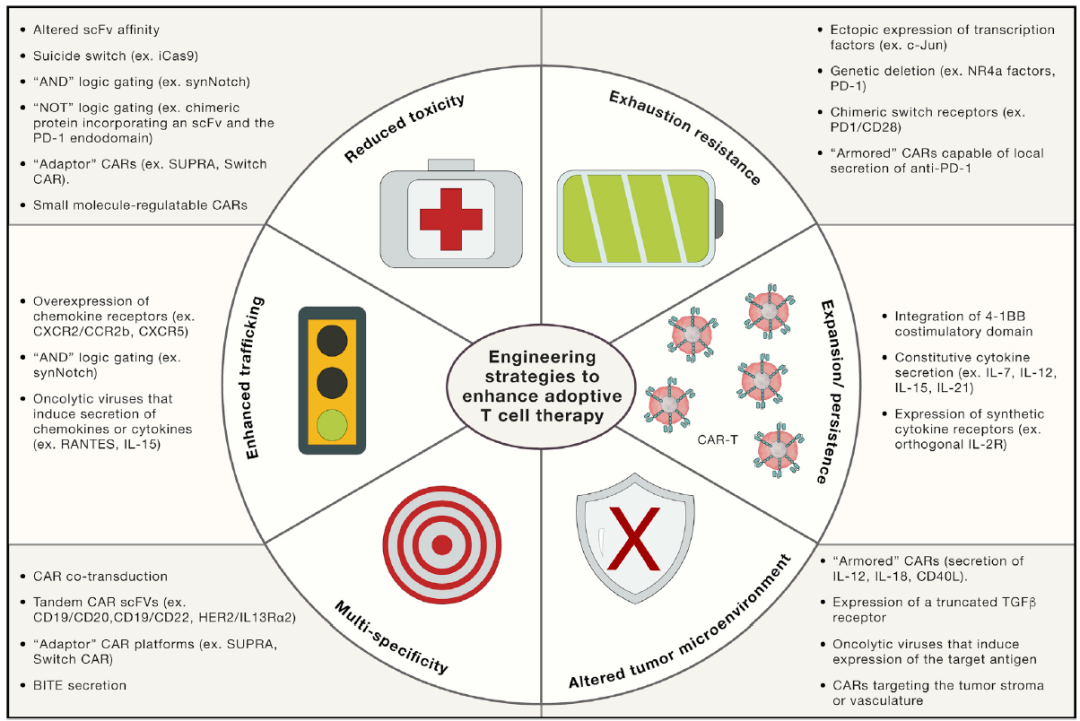
增强过继性T细胞疗法的工程策略
目前,增强T细胞疗法的效力有两种方法:增强特异性和增加安全性。
-
开发自杀开关,AND门控和适配器CAR平台以减轻CAR介导的毒性。c-Jun的异位表达或NR4a因子的基因缺失使CAR T细胞具有精疲力竭性,可能会改善实体瘤的疗效并增强持久性。
-
开发CAR-T细胞,使其分泌特定的因子以增强扩增或持久性(例如,IL-7,IL-12,IL-15或IL-21),减少对淋巴结清扫方案的需要,抵抗抑制性肿瘤微环境(例如,IL-18的分泌,截短的转化生长因子β[TGF-β]受体的表达),或充当肿瘤特异性的药物递送载体(例如,抗PD-1的局部分泌) 。
参考文献:
The Emerging Landscape of Immune Cell Therapies. Cell, 181(1), pp.46-62.
扫描上面二维码在移动端打开阅读