近日(5月31日),BioMarin宣布更新其在研血友病基因疗法valoctocogeneroxaparvovec(ValRox)一项开放标签I/II期临床研究的结果。新的数据已经提交给将在今年6月14-19日举办的世界血友病联盟(WFH)虚拟大会。
根据Biomarin,6e13vg/kg组4年更新数据和4e13 vg/kg组的3年更新数据显示,两组患者在接受单剂量ValRox治疗后不需要预防性因子VIII治疗。此外,两组患者中,累积平均年化出血率(ABR)均低于1,并且低于治疗前的基线水平。6e13 vg/kg组第4年的平均ABR为1.3,而4e13 vg/kg组第3年的平均ABR为0.5。过去的一年中,6e13vg/kg组7名参与者中的6人,4e13 vg/kg组6名参与者中的5人没有发生自发性出血。使用ValRox治疗后,因子VIII活性水平的下降情况与之前所观察到的一致,并保持在一个可以提供止血效果的范围内。
安全性表现与之前的报道数据一致,没有延迟发生的治疗相关事件。受试者没有产生对因子VIII的抗性,没有人退出研究,没有发生血栓事件。与使用ValRox相关的最常见不良事件发生在早期,包括短暂的输液反应和通过肝功能测试检测到的某些蛋白质和酶水平的轻中度提升,这些不良事件都没有长期的临床后遗症。
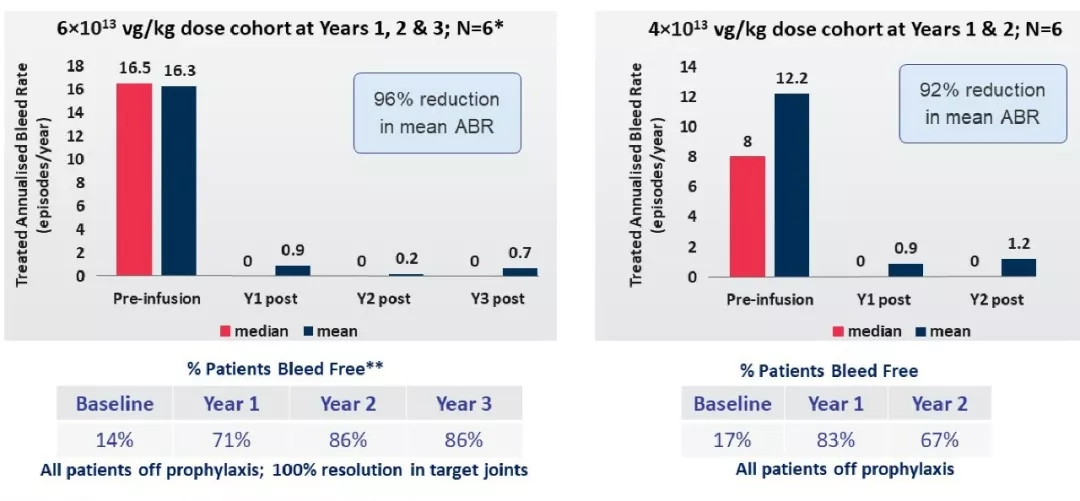
去年(2019年7月),BioMarin在ISTH上公布了ValRox的I/II期临床研究结果。根据公告,这项代号BMN270-201的I/II期临床研究包含了6e13 vg/kg和4e13 vg/kg两组研究数据。数据显示6e13 vg/kg组6位患者治疗三年后的平均ABR从入组前的16.3降至0.7,降幅达96%,中位ABR从入组前的16.5降至0,86%的患者未发生出血事件,同时所有的患者都不需要进行预防治疗。4e13 vg/kg组6位患者2年数据表现出略差于6e13 vg/kg组的结果,治疗两年后平均ABR从入组前的12.2降至1.2,降幅92%,中位ABR从入组前的8降至0,67%的患者未发生出血事件,两组患者都不需要预防治疗。
Valoctocogene roxaparvovec
ValRox全称Valoctocogeneroxaparvovec(曾用名BMN270),是一种利用AAV5病毒载体将编码凝血因子VIII基因的功能性拷贝递送到患者体内的基因疗法。该疗法可以帮助患者恢复自身凝血因子VIII生产能力,达到“一劳永逸”治疗A型血友病的效果。
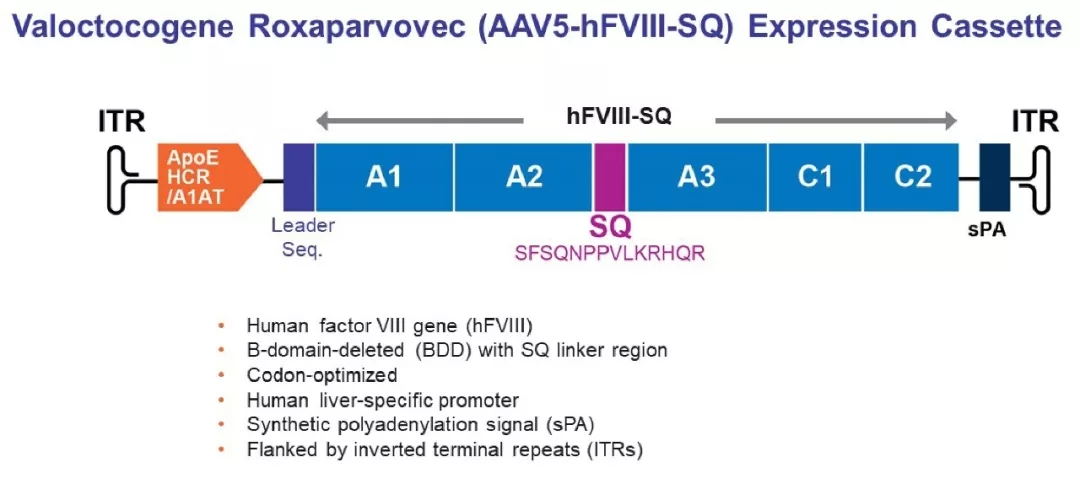
ValRox采用AAV5载体,为满足AAV5的装配要求,BioMarin删除B结构域,使FⅧ基因由7kbp减少至约4.4 kbp,A2和A3结构域通过SQ序列进行连接。删除B结构域的因子VIII可保留活性,目前已有多个删除B结构域的重组因子VIII上市(如NUWIQ、ReFacto和XYNTHA)。BioMarin还对因子VIII基因还进行了密码子优化,设计了末端反向重复序列(ITRs)、人体肝脏细胞特异性的启动子以及sPA。
百万美元天价基因疗法是否值回票价?
在与血友病的千年抗争史中,人类取得了长足的进步。随着上世纪50年代凝血疗法的出现,如今血友病患者在正常情况下可以享受与常人几乎无异的生存时间。然而,现有的疗法每周需进行2-3次用药,并且依然存在潜在的出血风险,给患者的日常生活带来很大困扰。此外,血友病患者凝血因子VIII预防治疗开销不菲,儿童患者一生开销可以轻易达到数百万美元。
而基因疗法作为一种“一劳永逸”的治疗选择,有望改善血友病的治疗方式。不过与其他基因疗法类似,根据BioMarin透露,ValRox的定价预计在每次治疗200万-300万美元之间,这一价格已经超过了同为基因疗法的全球最昂贵药物Zolgensma。
毫无疑问,目前的实验数据显示ValRox将成为血友病治疗的革命性产品。但面对百万美元的治疗费用,ValRox是否真的能值回票价?这种担心并不是空穴来风,早在研发过程中,ValRox就多次遭到了有关持续性问题的质疑。
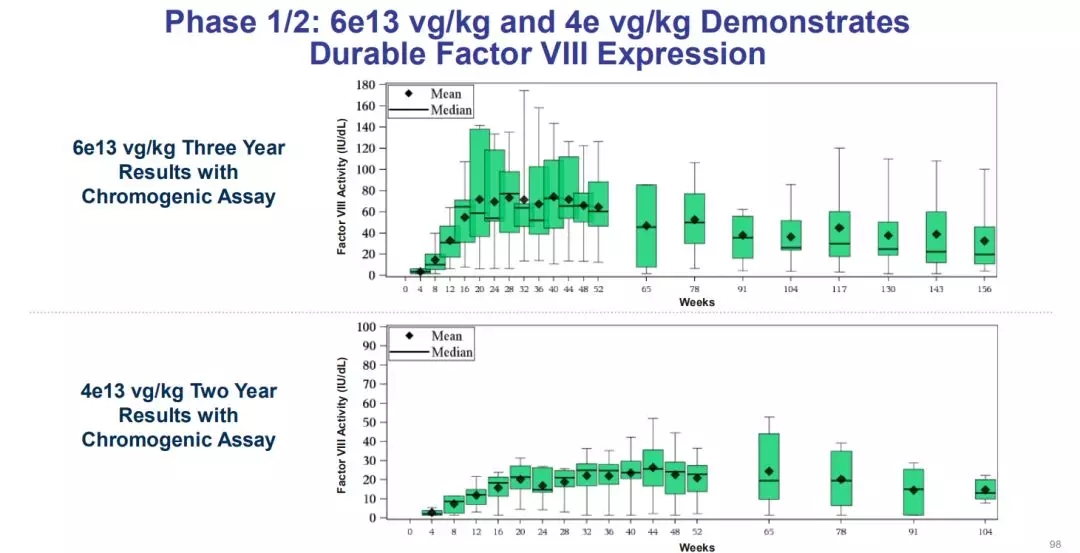
△患者因子VIII水平变化
由此,我们可以看到一个治疗后因子VIII活跃水平的不断下降趋势,即注射后第一,二,三年,患者的平均因子VIII活性水平分别为64.3,36.4和32.7IU/dL。
事实上,ValRox是否值得如此高昂的治疗费用是个综合性问题,至少目前看来持续性挑战“瑕不掩瑜”。严重血友病患者因子VIII活性水平一般低于1 IU/dL,可能会发生肌肉或关节的自发性出血。1 IU/dL至5 IU/dL是中度血友病,偶有自发性出血,在小手术或外伤情况下可能发生严重出血。而5 IU/dL至40 IU/dL是轻度血友病,罕有自发性出血,在大手术或外伤情况下可能发生严重出血。通常医生们认为因子VIII活性水平在12 IU/dL,就可以限制出血风险。
诚然,利用基因疗法治疗血友病的最理想目标当然是让患者的因子VIII活性水平保持在40 IU/dL以上,但12 IU/dL同样具有重大的治疗意义。就算只有5 IU/dL也可以显著降低血友病严重程度,减少患者对预防性注射的需求。因此,ValRox第三年的因子VIII活跃水平依然能很好的减少患者出血风险和对凝血因子输注的需求。
去年,由于对有效性持续时间的担心,BioMarin获得了广泛的关注。然而在其公开该疗法预计200-300万美元的治疗费用后,人们对于价格的关注已经大于对于疗法本身的关注。BioMarin CEO曾表示,公司已经证明200-300万的价格依然是合适的,并且提出“即使疗效耗尽,新的技术也可以给再次治疗提供可能。”
血友病基因疗法之争
2019年8月,BioMarin宣布放弃低剂量ValRox的开发,理由是“绝大多数患者更适合高剂量治疗”。事实上,这也是BioMarin力图将ValRox第一个推向市场的表现。BioMarin研发部主任Henry Fuchs曾表示,在ValRox率先获批后,竞争对手们快速审批的机会将变得渺茫,这将为公司争取极大的市场优势。
然而这种不惜一切代价争第一的做法,也被认为是一种“赌博”。原因是ValRox本身的持续性问题和来自于竞品的压力,尤其是Sangamo/Pfizer旗下的SB-525有着更快的起效时间(5-7周),而VolRox通常要在第4个月才能使患者的因子VIII水平恢复正常。因此BioMarin携有“瑕疵”的产品率先上市,以期抢占血友病市场的做法虽然能带来先发优势,但对于基因疗法这种全新的治疗手段,“先发or 疗效”的胜负犹未可知。根据BioMarin预计,该疗法有望给公司带来每年100-150亿美元收入。
目前,BioMarin的PDUFA日期是8月21日,没有任何审查小组在最后一刻提出任何问题。
然而无论ValRox最终表现如何,随着更多基因疗法的加入,血友病治疗和价值百亿美元的市场格局终将会被改写。
两款同类在研产品
Sangamo/Pfizer & SB-525
2019年7月召开的ISTH 2019上,Sangamo和辉瑞宣布重度A型血友病基因疗法SB-525的I/II期Alta临床研究结果。此次研究一共入组10位患者,并将其分为4个剂量爬升组, 9e11 vg/kg (2位患者), 2e12 vg/kg (2位患者),1e13 vg/kg (2位患者)和3e13 vg/kg (4位患者)。
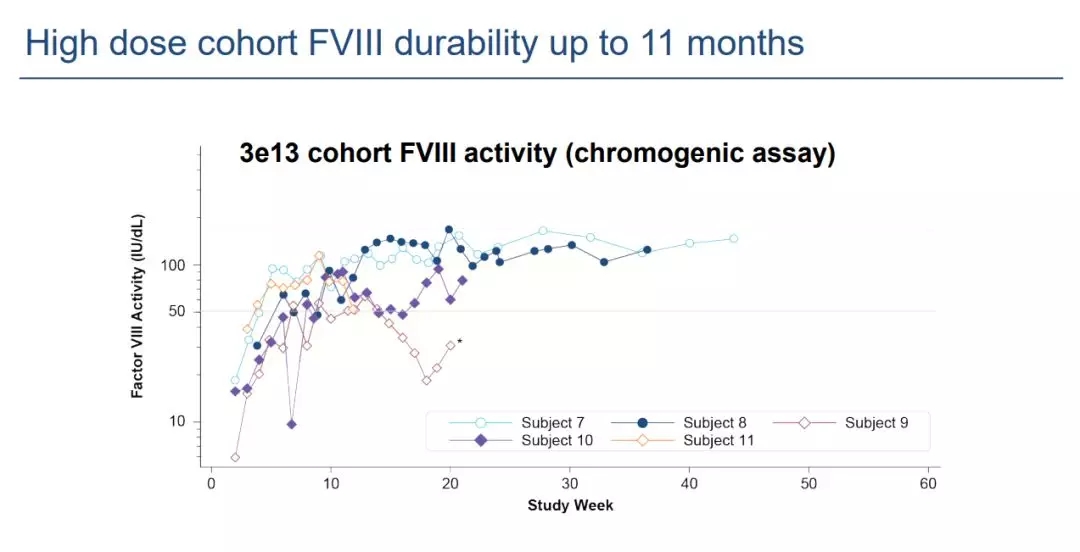
数据显示,使用SB-525时,患者的凝血因子VIII水平呈现剂量依赖性上升;使用凝血因子VIII替代疗法时,患者的凝血因子VIII水平呈现剂量依赖性下降。在1e13vg/kg剂量组中,两位患者的凝血因子VIII活性水平分别在52周和32周内都保持稳定。在3e13vg/kg剂量组中,4位患者分别接受了为期24周、19周、6周和4周的随访。前两位患者(7号患者和8号患者)分别在24周和19周随访中保持了凝血因子VIII正常水平,后两位患者(9号患者和10号患者)分别在6周和4周随访中展现出了与7、8号患者相似的凝血因子VIII活性水平上升模式,即使用SB-525后,患者凝血因子VIII水平可以在较早时间点达到正常水平。
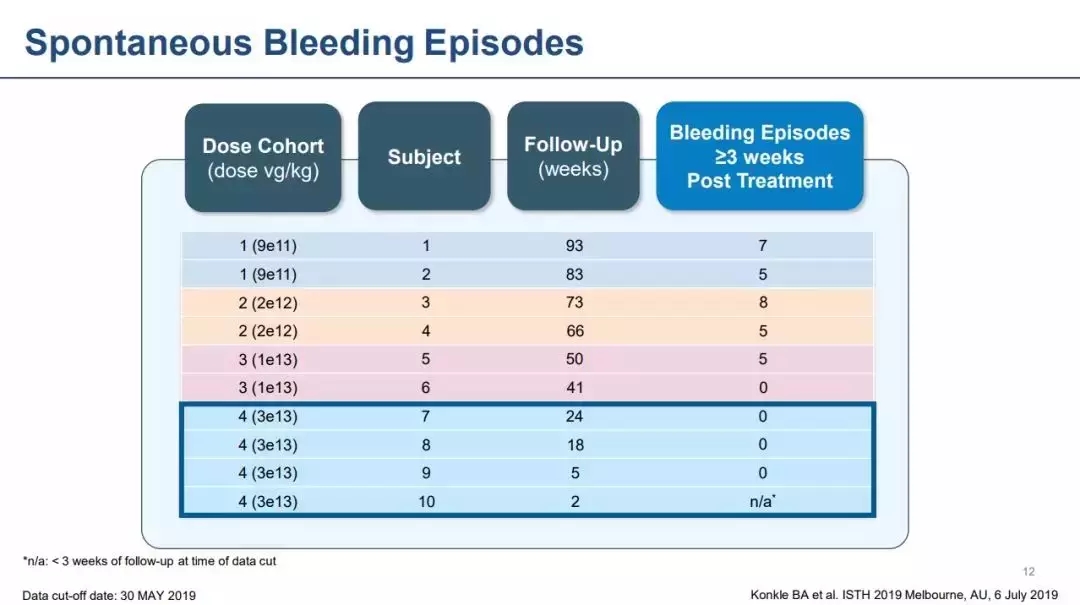
注:文中数据和截图PPT数据不同的原因是ISTH会议数据收集截止期为5月30日(即PPT数据截点),而文中所采用的数据截点为6月18日(即公司7月公开试验数据截点)。
安全性和耐受性方面,SB-525总体表现良好。Alta研究中所有入组者都没有接受预防性类固醇治疗。此外,一起与治疗相关的严重不良事件(SAE)被上报,该患者在接受SB-525输注后的第六小时出现低血压和发热症状,经治疗后按计划在24小时内出院。后续完成注射的3位患者均未出现类似的低血压症状。
今年10月,Sangamo R&D日更新了Alta临床研究结果。结果显示SB-525在11位受试者中耐受性总体良好。所有与治疗相关的转氨酶(ALT)升高均控制在低水平上,到目前为止,无一例与因子VIII表达缺失相关。与7月时结论相同,与基线相比,因子VIII活性呈剂量依赖性增加。观察到3e13vg/kg高剂量组患者的因子VIII水平在第5-7周可以达到正常,并且效果在第11个依然保持较高水平。而在安全性方面,高剂量组治疗过程中没有出现过出血事件,也不需要凝血因子替代治疗。
扫描上面二维码在移动端打开阅读