免疫学的世界,实在太奇妙了,得做好认知三天两头就被刷新一波的准备。
上个月奇点糕们就介绍过,先天免疫细胞也会形成抗原特异性的免疫记忆,这种发现刷新的认知幅度,甚至足以改写免疫学教科书。而今天的这个新发现虽然没那么惊人,却也是很有趣和新奇的。
加州大学旧金山分校的研究团队发现,在抗肿瘤免疫过程中,负责加工处理抗原,并将抗原呈递给杀伤性T细胞的树突状细胞(Dendritic Cells, DC),竟然是通过形成外泌体囊泡的方式,完成这一整个过程的。
具体来说,肿瘤微环境中的迁移型树突状细胞(mDCs),会用囊泡把抗原带出来,交给淋巴结中的组织驻留型同伴(rDCs),由它们激活CD8+/CD4+T细胞。如果不能形成囊泡,T细胞就无法被激活[1]。
这项研究发表在Cancer Cell上。
树突状细胞对抗癌免疫有着深远的影响,而这种影响主要是通过加工-处理-呈递抗原的流程施加的。奇点糕们此前也介绍过,限制这个过程中树突状细胞对抗原的提前降解,就能显著提升免疫治疗的疗效。
但是这个过程中,还有很多的未解之谜,比如说抗原呈递的具体途径就众说纷纭。有研究就以抗结核杆菌感染的免疫为模型,认为抗原是直接以可溶蛋白质的形态,被树突状细胞释放出来,再被T细胞摄取的[2]。
但也有研究提出了一种名为“变装”(cross-Dressing)的途径,在这个过程中,树突状细胞会捕获肿瘤产生的外泌体,然后让抗原从外泌体表面向自己的细胞外膜转移,相当于直接把抗原披在了身上,才得名“变装”[3]。
这些听起来就很有趣的途径,也体现了加工-处理-呈递抗原流程的复杂。再加上树突状细胞本身也能分出许多类型,不同类型的功能存在差异,想要明确整个流程绝非易事。
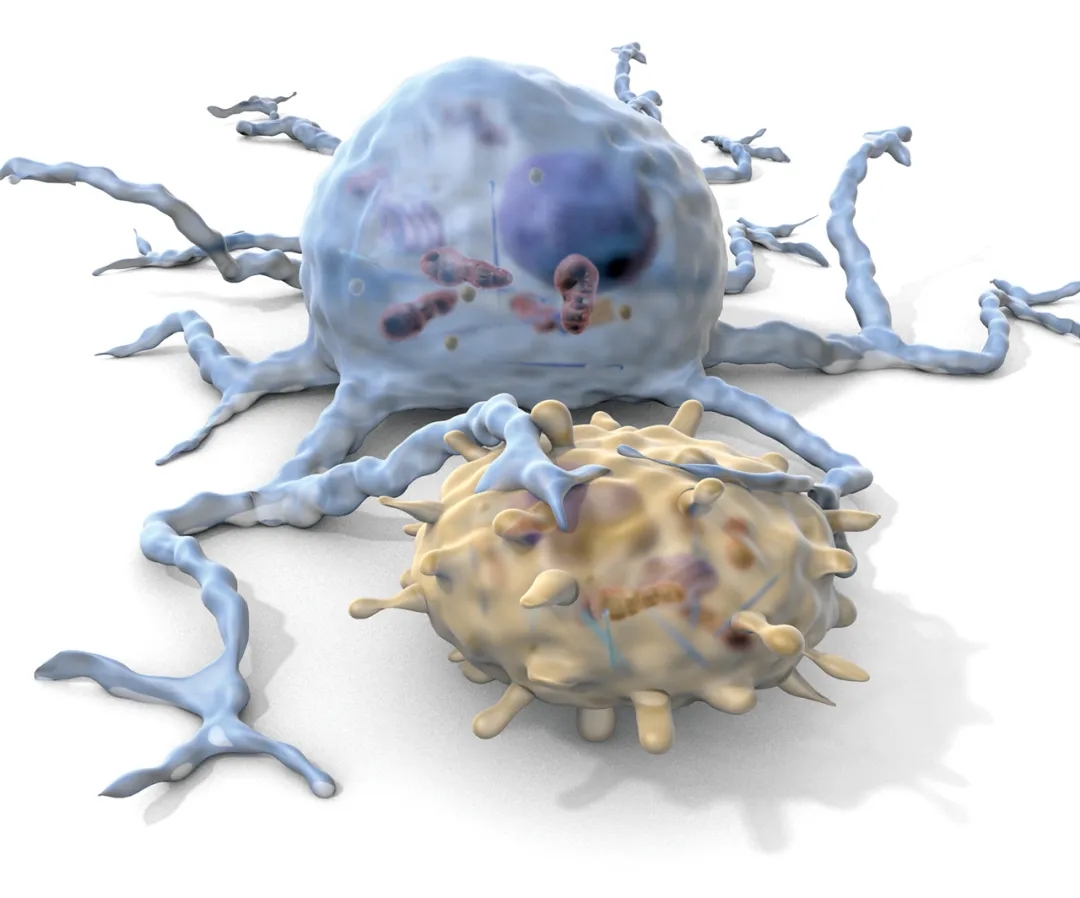
树突细胞(蓝)向T细胞(黄)呈递抗原的过程,姿势挺奇妙的
(图片来源:《科学》)
而在本次的研究中,加州大学旧金山分校的研究团队想到了一个巧妙的方法——对抗原中的部分蛋白质进行荧光染色,从而追踪并且重现抗原经历的每一幕,这样不就能明确流程了吗?
在黑色素瘤小鼠模型上进行的实验很快显示,肿瘤微环境中的肿瘤相关巨噬细胞、单核细胞、以及两种不同亚型的树突状细胞,基本上卷走了全部被荧光染色标记的抗原。
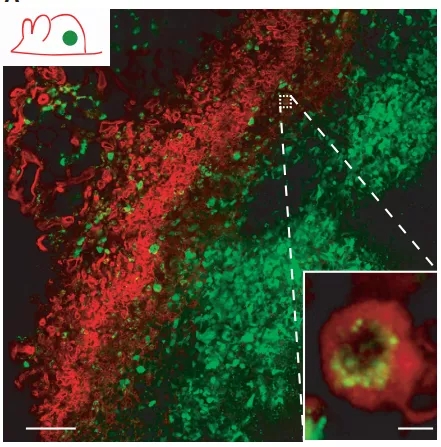
但让研究团队惊讶的是,这些抗原在树突状细胞当中,都是被囊泡结构所包裹的,就像下面这张图里一样。整体来看,大约有40%的树突状细胞里存在被染色的抗原,包括了迁移型和组织驻留型两大不同亚型。
放大,看右下角~
这些满载而归的树突状细胞,接下来会进入肿瘤相关的引流淋巴结(Draining Lymph Nodes),进行呈递抗原这一步。但到了淋巴结,树突状细胞并不会简单地把抗原扔给T细胞,就算完事儿了。
呈递过程的第一步,是不同的树突状细胞亚群之间,也就是迁移型亚群(mDCs)和驻留在淋巴结中的亚群(rDCs),彼此紧密联系形成突触,让抗原在囊泡中先进行内部传递,也就是一开头动图中呈现的那一步。
完成内部传递之后,不同亚群的树突状细胞,才会各找各的目标去呈递抗原。比如rDC1型和2型,以及mDC1型的树突状细胞,就去负责激活CD8+T细胞,而只有mDC2型树突状细胞,能够激活CD4+T细胞。
如果这些树突状细胞不能形成囊泡,那就没办法激活对应类型的T细胞啦。而且研究团队还发现,mDC1型树突状细胞在突触形成那一步中,抢夺抗原的能力明显比mDC2型要强,具体机制与PI3K激酶有关。
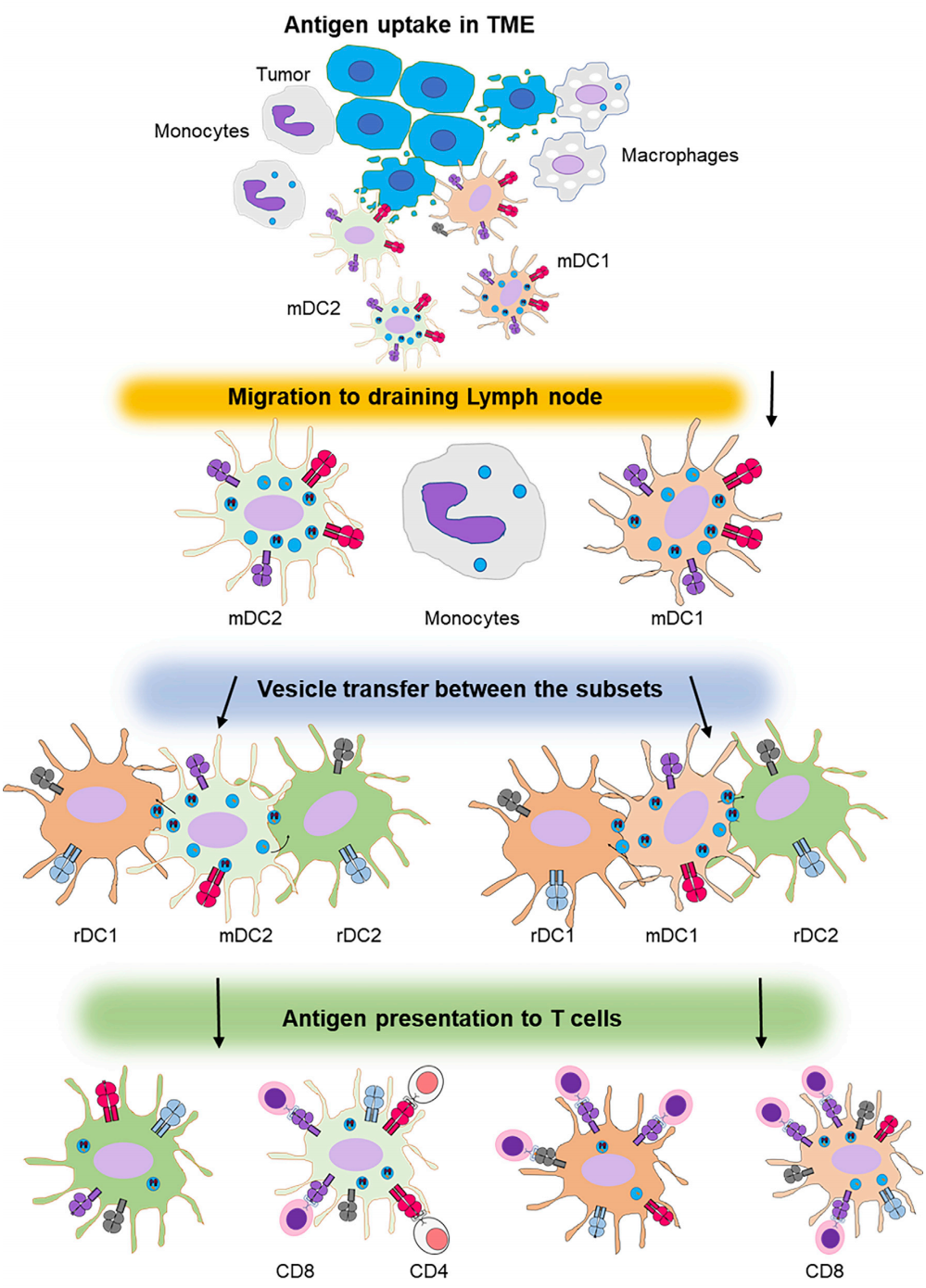
整个流程可以用这张图概括
新奇的“囊泡机制”,再次提示了树突状细胞提呈抗原的复杂性,不过研究并没有对囊泡能否影响抗肿瘤免疫应答的强度,去作进一步的分析。
不过Cancer Cell配发的社论指出,既然树突状细胞的囊泡和CD8+T细胞激活有明确的关系,那后续研究就得安排上,如果能从这个角度放大免疫治疗的疗效,那也是极好的[4]。此言甚善,给安排一个!
参考资料:
1.Ruhland M K, Roberts E W, Cai E, et al. Visualizing Synaptic Transfer of Tumor Antigens among Dendritic Cells [J]. Cancer Cell, 2020, 37(6): 786-99.e5.
2.Srivastava S, Ernst J D. Cell-to-cell transfer of M. tuberculosis antigens optimizes CD4 T cell priming[J]. Cell Host & Microbe, 2014, 15(6): 741-752.
3.Wakim L M, Bevan M J. Cross-dressed dendritic cells drive memory CD8+ T-cell activation after viral infection[J]. Nature, 2011, 471(7340): 629-632.
4.https://www.cell.com/cancer-cell/retrieve/pii/S1535610820302634
头图来源:Pixabay
扫描上面二维码在移动端打开阅读