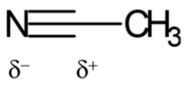一个负责将复杂组分尽量得分开,另一个通过分子量这个固有内标将化合物一个一个检测并定性定量;强大的分离能力加上强大的检测能力,就是LC-MS的无敌之处。
近年,化学合成的药物分子数量逐渐达到极限,而生物药由于其与疾病靶点天然的契合性,不但可以补充化学药物的缺口,还能实现更好的治疗效果,成为医药行业的新风口。这其中,蛋白质药物无疑是生物药研发中的热点,那么建立高通量、灵敏、准确的蛋白质药物定量分析方法就成了药物研发的关键前提。
与传统化学药相比,生物药成分更复杂,纯化更困难。在质量检测方面,由于采用生物发酵方法获得产物,对杂质、次级代谢产物、内毒素残留和核酸残留等,都要进行更严格的检验。这无疑对传统检测分析方法提出了更高的要求。高效液相色谱具有对成分复杂样品的高效分离能力,而质谱具有高选择性,要灵敏度,能够提供相对分子质量和分子结构信息。本文将重点分析LC-MS系统的流动相方法开发相关关键因素。
流动相的可选范围非常宽泛,这令流动相的选择难度远远大于固定相的选择难度,然而在实际的方法开发中,还是有方法可以极大的缩小选择范围,聚焦于成功几率更高的流动相条件。
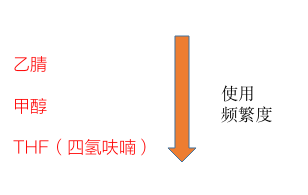
典型的反向流动相是由弱溶剂(如水或缓冲体系)和强有机溶剂(如乙腈、甲醇或THF)共同组成的,那么乙腈或甲醇是最常用的两种有机溶剂。
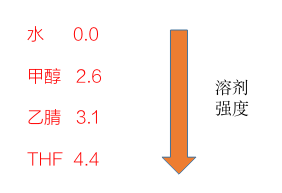
溶剂的疏水性,决定了它们洗脱能力的强弱,而溶剂的洗脱能力,又决定了被洗脱化合物所需的溶剂量,常用溶剂中,疏水性能的排列是乙腈大于甲醇大于水,所以乙腈是洗脱能力最强的溶剂。
溶剂的洗脱选择性,是由溶剂的官能团决定的,甲醇溶剂既是氢键的强质子供体,又是强质子受体。甲醇的洗脱能力比乙腈弱,大概同时粘度大,当小颗粒长柱子的柱中高速流动时会产生较高的柱压。不过在苯基柱中,甲醇因能体现出苯基柱特有的pi-pi键选择性,而实现更好的分离性。
乙腈是具有偶极矩的分子,氢键受体则非常弱。乙腈具有很多优良特性,是很多高效液相色谱中的理想溶剂,乙腈在混合体系中粘度较低,相对柱压就较低,乙腈的紫外截止波长为190nm,在很多化合物测定波长处是没有紫外吸收的,同时还有强洗脱性,缺点是价格较贵。
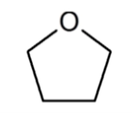
THF四氢呋喃可以接受氢键的质子,但不是氢键的质子供体。
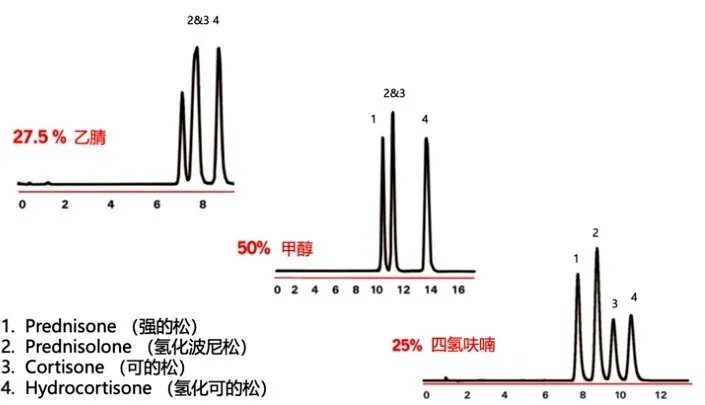
用乙腈,甲醇,THF分别对相同的四种类固醇类物质进行分析,色谱图显示了三种溶剂间的选择性差异。
虽然可用的缓冲液种类的有很多,但常用的缓冲液并不多,同时要根据样品的实际条件,对各种缓冲液进行选择。
在确定流动相pH时,要充分考虑目标物在环境中的稳定性,
缓冲体系的pH过低,是否会引起色谱填料的水解?比TFA更强的酸会导致色谱填料的水解,硅羟基的暴露也会导致保留效果变差,同时不同厂家,不同品牌的填料,对于溶剂pH的要求也不相同,这些都是在工艺开发、转移、放大时需要考虑的。
pH过高时,硅胶会发生溶解,一般硅基相在pH 8左右保持稳定,如果缓冲液pH在10左右,则需要对化学键进行保护处理,当pH升高到12左右,则需要含有有机硅杂化键的硅胶。
所以当我们为反向LC-MS选择流动相时,尽量避免使用强酸和强碱,如TFA会抑制信号。使用挥发性缓冲液代替磷酸盐。尽可能使用最好质量的水,如购买LC-MS级水,不使用超过一周的水相流动相。
值得注意的是,在HPLC中使用的许多缓冲液在 LC-MS中都不能使用,如TFA和磷酸盐缓冲液,对质谱分析有影响,所以需要用甲酸,乙酸胺来代替使用在LC-MS中。
酸性样品pH流动相以下2个单位左右,在反向条件下保留效果更好,离子化状态可以得到更好的峰型,同时减少次价离子键相互作用的机会,但对于保留时间相对靠后的峰宽可能有影响。碱性样品与之相反。
相同的pKa是一个需要避免的pH区间,由于此时物质以不同浓度同时存在于水相和疏水相中,这会造成物质的色谱峰变宽和不对称,而且次价键的相互作用的可能性很大。这和碱性样品性质相同。
酸性样品同样应该避免的区间,与低pH相同,此时样品同时存在于水相和疏水相中,同样会造成物质的色谱峰变宽和不对称,而且次价键的相互作用的可能性很大。碱性样品则与之相反。
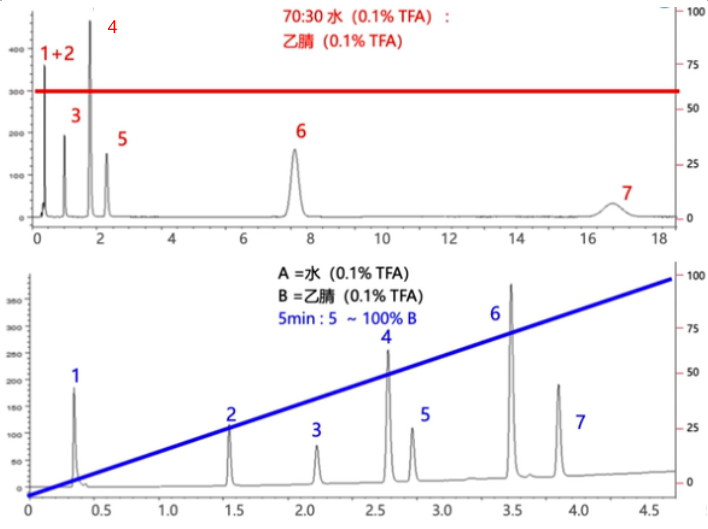
梯度洗脱是用来分离同一色谱中疏水性差异较大的物质,这些物质在相同时间长度的等度洗脱时是无法分离的。梯度洗脱可以让峰型更窄,适合定量,并改善强度小,洗脱完的色谱峰的检测。同时梯度洗脱对于色谱柱的清洗,和再生非常方便,也有利于对于被分析物的条件摸索。
梯度洗脱是的斜率变化,类似于等度洗脱时溶剂的强度。增大梯度洗脱的斜率或等度洗脱的溶剂强度,都可以减少分析时间,但也会降低分辨率。反之亦然。同时这两者也会影响选择性。梯度洗脱的目的就是在分析时间最小化的时候获得最优化的分辨率。
我们可以看出,梯度洗脱的分辨率更好,特别是峰1和峰2的分离,同时梯度洗脱也节约了更多分析时间。
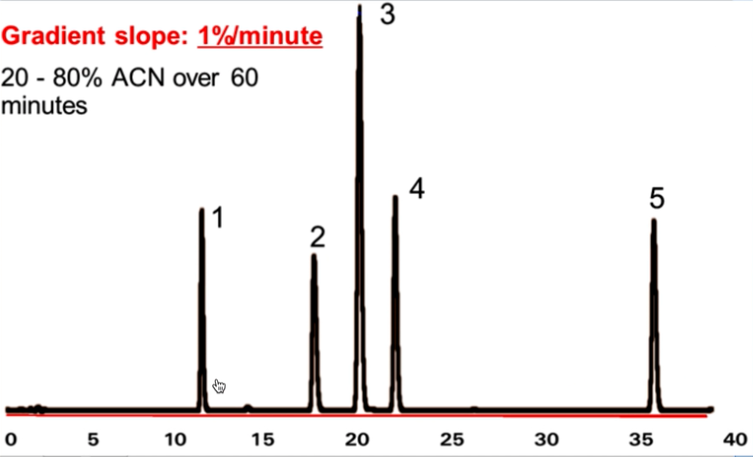
初试梯度用来测试分析物的洗脱时间,如在60min内,有机相从20%变化到80%。
调整有机相递增浓度,能够调整早洗脱物质的出峰时间,减少分析时间。如以2、3、4%/min的递增速度洗脱。
同时,调整起始有机相的浓度,可以在出峰时间和分辨率两者中取最优方案。如以20%、30%浓度的有机相作为起始浓度。通常会对有机相浓度进行不断优化,以获得最高得分辨率和最少的分析时间。
影响色谱柱清洁的环节是梯度末有机相浓度%的优化。如在柱清洁时显等度保持10min,然后将有机相浓度%梯度增加至90%保持2min,然后回到起始条件保持3min以平衡色谱柱,再进下一针样品。
由于温度对HPLC的选择性的影响没有稳定规律,所以在方法开发时就一定要对温度特别注意。温度较高时能降低流动相粘度和柱压,适合于流速更高、柱长更长、颗粒更小的柱子。与室温相比,将高的温度也能减少洗脱时间和提高方法的重现性。不过这样的影响需视样品实际情况而定,复杂样品的分离,温度的选择只有相对优化,并没有绝对改善。
一般的方法开发,是以30摄氏度为初始温度进行色谱柱的筛选,流动相的选择与优化。只有在需要减少柱压、或分辨率不能满足需求时,才会提高使用温度。
本文为大家梳理了与方法开发相关的流动相组成,包括如何根据溶剂强度和洗脱强度来选择溶剂,还在缓冲溶液的选择部分阐述了pH的重要性,对比了等度洗脱和梯度洗脱的特点,以及梯度洗脱的方法建立。以及温度对与方法的影响。

扫描上面二维码在移动端打开阅读