2020年8月15日/医麦客新闻 eMedClub News/--昨日,据国家药监局药品审评中心(CDE)官网显示,北京三有利和泽生物科技有限公司和首都医科大学联合申报的人牙髓间充质干细胞注射液的新药临床试验申请获得默示许可,适应症为:慢性牙周炎,如慢性牙周炎所致的牙周组织缺损。
就在不久前结束的由医麦客主办的2020 BPIT 生物创新药技术大会——第二届国际干细胞产业转化领袖峰会分论坛上,来自三有利和泽生物的技术和质量总监孙彦洵博士针对这款牙髓来源的间充质干细胞的IND申报、质量控制以及干细胞治疗产品IND申报过程中需要注意的问题和解决策略做了精彩分享,为业内提供了极具参考价值的建议。
牙髓干细胞(DPSCs)是一种具有多能分化和自我更新能力的间充质干细胞,来源于正常人牙髓,相比广为熟知的脐带血干细胞、脊髓干细胞,牙髓干细胞是在2000年由Gronthos 、施松涛教授课题组发现并分离,因为成牙潜能突出,预想中的医学应用场景主要是用于治疗牙周病等口腔疾病,同时在自体生物牙根的制备及骨损伤修复等方面也将有广阔的应用前景。
不仅对口腔疾病治疗效果好,安全性无副作用,DPSCs对全身性疾病也极具应用前景。大量研究表明,DPSCs对脊髓损伤、帕金森病、阿尔茨海默病、脑缺血、心肌梗死、肌营养不良、糖尿病、肝病、眼病、免疫疾病、口腔疾病等多种疾病均有疗效。也有报道称,DPSCs比骨髓间充质干细胞(典型的间充质干细胞)具有更高的再生潜能。因此,DPSCs近年来备受关注。
尽管目前还存在诸多挑战,包括影响机制、建立临床使用的细胞处理和移植方法,但由于DPSCs具有自我更新和多向分化的能力、易于通过无创方法分离,且不存在伦理问题,DPSCs极具潜力成为多种临床应用的干细胞来源。20119年3月,日本大阪牙科大学在《国际分子科学杂志》发表了一篇探讨牙髓干细胞治疗各种系统性疾病的临床潜力及进展的报告。
国内今年已有8款干细胞获得临床许可
在我国,干细胞按药品、技术管理的“双轨制”监管。企业的干细胞制剂鼓励按药品申报,由国家食品药品监督管理总局(NMPA)监管;医疗机构主导的生物医学新技术,即医院制剂可按医疗技术进行管理,由卫健委监管。因此,谈及我国干细胞治疗的临床进展,可以从干细胞临床研究备案项目和干细胞新药临床研究两个角度出发。
2017年发布的《药品注册管理办法(修订稿)》明确指出细胞治疗类产品可以按药品进行注册上市,紧接着《细胞治疗产品研究与评价技术指导原则(试行)》的颁布,更加明晰了细胞治疗作为药品申报的标准。
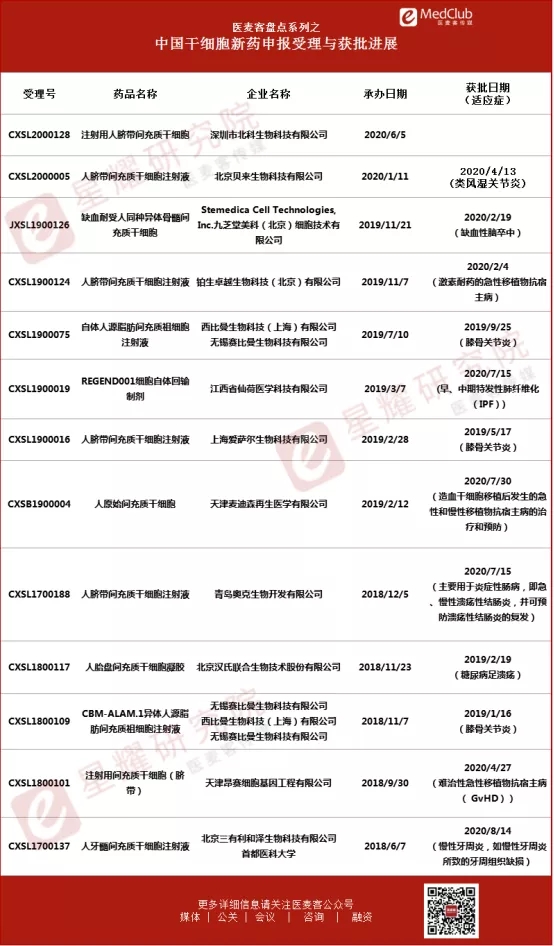
2018年6月至今,国内相继有13款干细胞新药的IND申请获国家药品审评中心(CDE)正式受理,除了江西省仙荷医学科技有限公司自主研发的REGEND001细胞自体回输制剂为自体肺基底层上皮细胞外,其它12款均为间充质干细胞。
而截止目前,受理的13款中有12款干细胞新药IND已经获得临床默示许可,除REGEND001细胞自体回输制剂外,其余获得临床批件的分别是胎盘、脐带、牙髓、异体/自体脂肪来源的间充质干细胞;尤其值得一提的是,这12款获准临床的干细胞产品中,有8款是获准于今年。
由此可见,尽管今年受疫情影响,但国内干细胞治疗领域的进展仍在继续,尤其间充质干细胞在此次新冠肺炎的临床治疗探索上也表现出极大的潜力,同时,我们还即将迎来美国FDA批准的第一个间充质干细胞疗法(Mesoblast公司的Ryoncil),日前,FDA的肿瘤药物咨询委员会(Oncologic Drugs Advisory Committee,ODAC)以8比2的投票支持Ryoncil的上市申请,提高了其获批的可能性。
此次,人牙髓间充质干细胞的临床试验许可,将进一步推动干细胞领域的全面发展,我们期待其临床试验能顺利展开。
参考资料:
1.CDE官网
2.Doi:10.3390/ijms20051132
3.https://endpts.com/fdas-odac-shrugs-off-objections-to-mesoblasts-gvhd-drug-for-children-voting-8-2-in-favor-and-improving-the-odds-of-an-approval/
扫描上面二维码在移动端打开阅读