中国上海—2020年8月24日,安源医药科技(上海)有限公司宣布,历时3年多研发的治疗非酒精性脂肪肝炎(NASH)创新生物药AP025获得美国FDA临床试验许可。
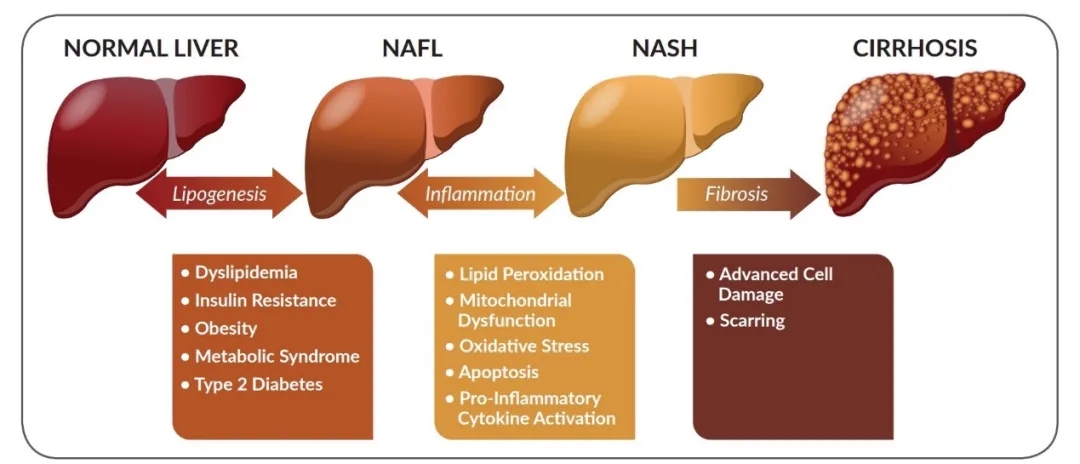
非酒精性脂肪性肝病(NAFLD)是肝细胞中脂肪过度堆积而导致的慢性肝病。随着肥胖及其相关代谢综合征的全球化流行,NAFLD已成为慢性肝病的重要病因,全球范围内NAFLD患者约占总人口的25%,其中15%~25% NAFLD患者发展为NASH,并随着症状的持续,约15% NASH患者进一步发展为肝硬化及肝癌,增加死亡风险。目前中国NASH患者约为4000万人,美国约为1500万人。尽管全球范围内NAFLD/NASH患者数量增长居高不下,但迄今为止NASH领域没有获准上市的治疗药物。
针对临床上未被满足的急迫药物需求,全球范围内多家企业布局NASH药物研发,大型药企如辉瑞、诺华、 默沙东、吉列德、诺和诺德、施贵宝、艾尔建等,生物科技公司如Intercept、Genefit、NGM、Inventiva、Viking、Galmed、Madrigal、Cymabay、Galectin等。clinicaltrials.gov 最新数据显示,目前全球有近百个NASH 药物处于临床开发不同阶段,如FXR激动剂奥贝胆酸、CCR2/5拮抗剂Cenicriviroc、SGLT-2抑制剂达格列净、PPARα/δ 激动剂Elafibranor、SCD-1抑制剂Aramchol、THR-β 激动剂Resmetirom、MPC调节剂MSDC-0602K等。基于国际NASH药物的研发大背景,中国多家生物医药公司积极投身其中,陆续有产品进入临床I-II期阶段。
2018年,Intercept、Madrigal、Viking 等多家公司相继公布了积极的II期数据,对多个NASH靶点进行了概念验证,给该领域带来一大波投资机会。然而时间到了2020年,多款处于临床中后期阶段的新药研发相继受挫,引发了整个NASH新药研发的市场震动。Intercept公司研发的FXR激动剂奥贝胆酸的III期临床试验结果显示,相对于安慰剂,10 mg和25 mg给药剂量下,纤维化改善且NASH症状未恶化的患者比例分别降低了5.7%和11.2%,并基于此结果提交了NDA。2020年6月,FDA认为该药基于替代组织病理学试验终点的预期益处仍不确定,且治疗获益未超潜在风险,因此不支持加速批准奥贝胆酸用于治疗NASH导致的肝纤维化。2020年7月,Genfit公司基于III期临床中期结果宣布终止Elafibranor治疗NASH与纤维化的继续临床研究,这一消息进一步打击了该领域的研发热情。
转折发生在2020年7月,新兴生物科技Akero公司公布了其从安进引进的一款长效FGF21衍生物Efruxifermin (AKR-001) 的II期临床结果。经过16周治疗后患者肝脏脂肪相对含量降低70%,78%患者NAS评分下降至少2分,48%患者至少改善一级纤维化、28%患者改善两级纤维化,治疗结果振奋人心,重燃NASH药物治疗的新希望。
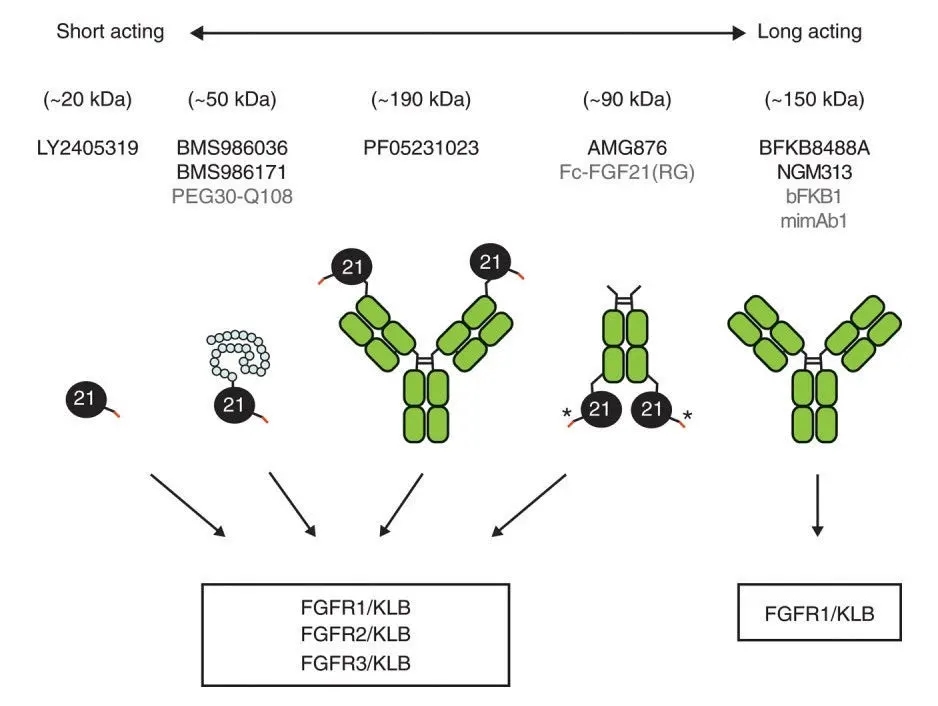
FGF即成纤维细胞生长因子,是一组具有保守结构域的信号蛋白,参与胚胎发育,组织再生和代谢稳态维持等。作为FGF家族的一员,FGF21是调节糖脂代谢的重要内分泌因子。动物水平的基础研究证明,FGF21通过促进脂肪酸氧化及抑制脂质新生,缓解肝脏脂肪变性,逆转或延缓肝脏炎性病变及纤维化发生发展。然而天然FGF21短暂的体内半衰期(0.5~2h)和较差的物化特性,限制了其作为候选药物。同时为了实现工业化生产及临床应用,只有通过改造FGF21以保留生物学活性并规避结构缺陷。全球范围内已有多家知名药企围绕FGF21开展研发布局多年,通过对FGF21进行点突变、PEG或Fc等长链融合、scaffold融合以及模拟抗体等技术修饰,开发出数款长效FGF21类似物。目前还没有FGF21药物上市,LY2405319、BMS986036、PF05231023、AKR-001、NGM313等产品均处于临床I-II期阶段。
全球在研FGF21受体激动剂
(FGF21-receptor agonists : an emerging therapeutic class for obesity-related diseases. Hormone Molecular Biology and Clinical Investigation)
与已进入临床的其它FGF21长效类似物不同,安源医药AP025是全球第一款进入临床的全人源、全长的FGF21长效蛋白,也是中国生物医药企业自主研发的第一款进入临床的长效FGF21产品。安源医药依托于自主知识产权的长效融合分子设计平台研制的AP025,在保留了人FGF21活性基础上,延长体内半衰期的同时,满足了工业化生产的需求,并在非临床研究中证明了其有效性和安全性。鉴于已有FGF21类似物在II期临床试验证了的靶点可行性,AP025显示出满足NASH/NAFLD药物治疗需求的积极潜力。
安源医药创建于2016年,致力于重组蛋白和治疗性抗体的源头研发,涉及代谢、肿瘤、凝血、抗病毒等治疗领域。安源医药立足中国,面向世界,已研发出多款具有Better-in-class潜力的新型大分子药物,具备从新药发现、工艺开发、成药性研究、临床前开发等全套能力。凭借自主研发的CHO细胞株高效开发平台、高亲和力抗体创制平台、超长效蛋白设计平台、双特异性抗体研制平台等通用型技术工具及技术转让、合作研究、联合开发等商业化思路,目前完成30个长效蛋白和抗体药物的概念验证,项目最快进入III期临床,期待安源医药后续能够深入推进和开发更多平价高端创新生物药,服务于中国患者。

扫描上面二维码在移动端打开阅读