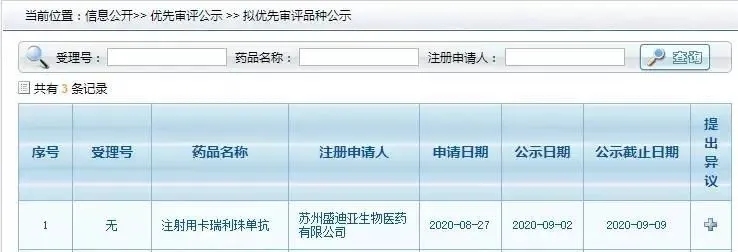
9 月 2 日,CDE 官网显示,卡瑞利珠单抗递交一项新适应上市申请,且被拟纳入优先审评(受理号暂未公布);根据恒瑞此前的公告,本次新适应症是联合顺铂和吉西他滨一线治疗局部复发或远处转移鼻咽癌。卡瑞利珠单抗新适应症的申请上市或许能让我们捕捉到一个讯息,即国内PD-1单抗市场的竞争愈发激烈。
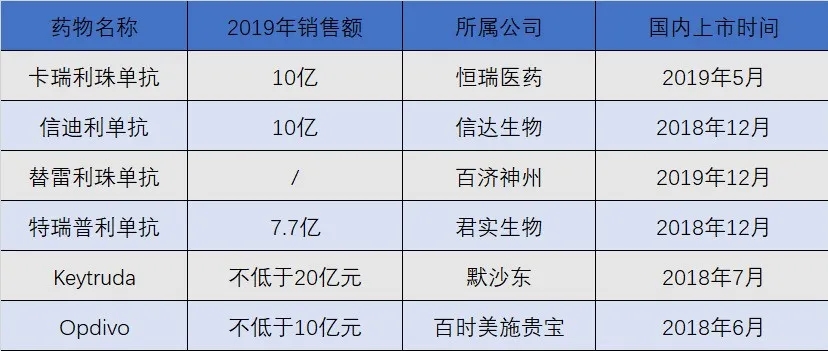
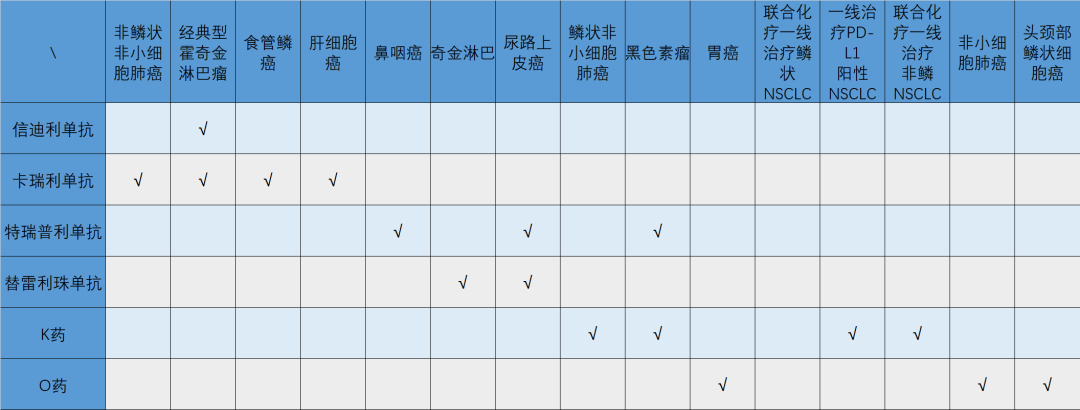
卡瑞利珠在国内获批之后于2019年7月底出货。不足半年销售中,卡瑞利珠销售额就已达到10亿元,表现抢眼。不过,国内市场PD-1单抗药物竞争同样火热。除了卡瑞利珠单抗,目前国内市场上已有6款PD-1单抗药,分别为百济神州的替雷利珠单抗、君实的特瑞普利单抗、信达的信迪利单抗,以及最早上市的K药、O药。
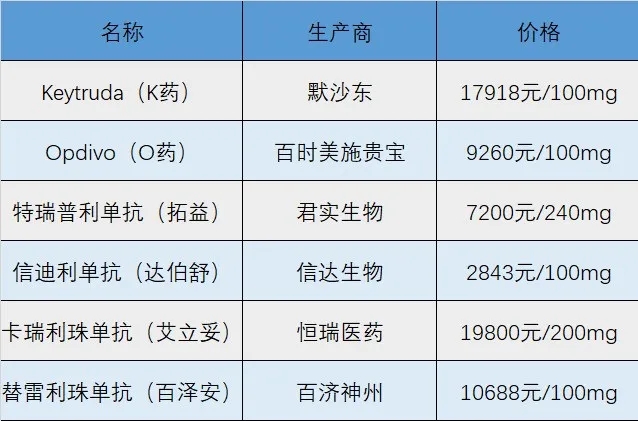
两款进口PD-1与四款国产PD-1形成了国内PD-1单抗的“4+2”竞争格局。面对硝烟四起的PD-1单抗市场,进口和国产厂家起初都希望通过低价占据先机,例如百时美施贵宝的Opdivo(俗称“O药”)和默沙东的Keytruda(俗称“K药”)售价均约为美国定价的一半,在几乎全球范围内都属于低价。
而信迪利单抗在2019年被纳入国家医保目录后,定价大幅下降,现在仅需2843元/瓶。尤其对于符合报销条件的霍奇金淋巴瘤患者经医保报销后,自付费用仅仅为原价的10%~50%。
其他未进入国家医保目录的PD-1产品则以另外的方式以实实在在的价格优惠获取市场。比如进入地方商业补充医保或开展慈善赠药项目,其中K药、O药和特瑞普利单抗就进入了佛山市商业补充医疗保险的“平安佛医保”。
百济神州则以慈善项目的方式突破价格底线。2020年3月,百济神州公布了替雷利珠单抗注射液慈善援助方案:买2援2,而后患者可灵活选择买2援2一年内循环,或买3援助至一年(最多不超过11个疗程),直到疾病进展或项目结束(以较早者为准)。据悉,百济神州替雷利珠单抗注射液的建议售价为10,688元/支(100mg)。这也意味着长期使用替雷利珠单抗注射液进行治疗的患者只需支付5个疗程的费用即可获得一整年的药物治疗,年治疗费用最低约为10.69万元。
当然,药物市场竞争向来不是单纯地以价格取胜。人才、销售实力、产能等都是药企间竞争的筹码。不过,要想让药物惠及更多的患者,占领更大的市场,更广泛的适应症才是在这场PD-1单抗竞争中拔得头筹的关键。
据相关数据统计,2020 年上半年,在中国申报上市的 28 个生物创新药中,有 15 项靶点来自 PD-1,而这些申报大多是为了更多得新适应症。2020 年以来,中国市场的 PD-1 药企们已然进入新一轮战争:全力拓展新适应症。
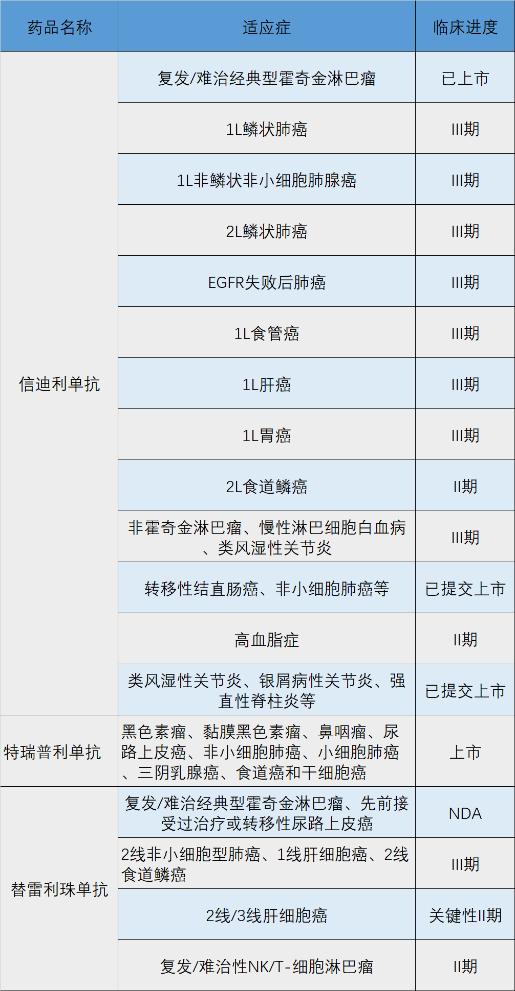
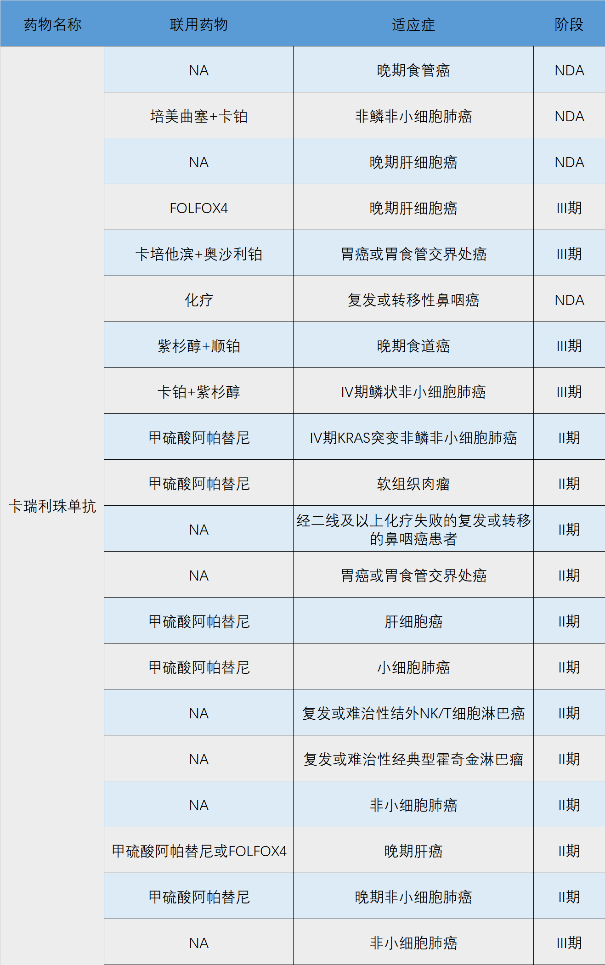
截至目前,恒瑞的卡瑞利珠单抗已在国内获批四个适应症:食管鳞癌、非鳞非小细胞肺癌、经典型霍奇金淋巴瘤、肝细胞癌。在临床布局上,卡瑞利珠单抗已登记的临床试验数量和适应症数量都是国产PD-1 单抗药物中最多的,在大适应症和药物联用上全面领先,适应症覆盖全面:在围绕SHR-1210 展开 15 项临床试验中,7 项为联合用药项目,包括了与化疗药物、阿帕替尼及MEK激酶抑制剂的联合治疗。
特瑞普利单抗是首款获批上市的国产PD-1单抗产品,目前获批上市的适应症为:黑色素瘤、鼻咽癌和尿路上皮癌。与信达生物、恒瑞医药的临床布局相比,君实生物特瑞普利单抗的开发则走了一条小众化的路线,专注于国内发病率较低而且临床缺乏直接治疗手段的适应症,优先开发了小众的黑色素瘤和鼻咽癌适应症,还布局了恒瑞与信达没有涉足的三阴乳腺癌、神经内分泌瘤等适应症。
2019年11月,K药在中国获批第四个适应症:转移性鳞状非小细胞肺癌(NSCLC)。在此之前,K药已在中国先后斩获3个肿瘤适应症,包括二线治疗黑色素瘤、联合化疗一线治疗鳞状NSCLC、一线治疗PD-L1阳性NSCLC。
2020年3月,百时美施贵宝宣布,O药已正式获得中国国家药品监督管理局批准用于治疗既往接受过两种或两种以上全身性治疗方案的晚期或复发性胃或胃食管连接部腺癌患者。这是继非小细胞肺癌、头颈部鳞状细胞癌之后,中国首个免疫肿瘤(I-O)药物欧狄沃在中国获批的第三个适应症。
目前,除了已上市的6款,国内市场还有共计15款处于临床或上市申请阶段的PD-1单抗药物。如誉衡药业PD-1赛帕利单抗注射液和嘉和生物的PD-1单抗杰诺单抗注射液等。在未来,随着更多企业的加入,国内PD-1单抗市场的竞争势必更激烈。
参考资料:
1. https://med.sina.com/article_detail_103_2_81501.html
2. https://www.sohu.com/a/411435092_177021

扫描上面二维码在移动端打开阅读