专注于开发p53小分子药物的PMV Pharma最领先产品还没进入临床,IPO当天市值就过16亿美元了。而目前靶向p53突变最领先的产品是Aprea Therapeutics公司的处于3期阶段,市值仅4.8亿美元,这到底怎么了?
1. PMV Pharma简介
2. p53背景
3. p53小分子激活剂进展
4. PC14586推进策略
5. 结语
PMV Pharma成立与2013年,是一家精准肿瘤公司,致力于发现和开发出治疗不限瘤种的靶向p53突变的小分子。该公司的共同创始人是Arnold Levine,在1979年发现了p53,正是基于40多年来对p53的认识,开发出了两个靶向突变型p53小分子,PC14586靶向Y220C突变,另一个靶向R273H突变,一个刚递交临床试验申请,一个还处于发现化合物阶段,IPO当天市值为16.13亿美元。
人类癌症中50%的癌症包含了p53突变,迄今为止,已经发现了超过25000个单一p53突变,它的突变会导致抑制肿瘤增殖的功能缺失,下图是突变频率排名前十的p53突变体。
图1 十大最常见的p53突变体(来源:PMVP招股说明书)
3 p53小分子激活剂进展
关于靶向p53的药物,主要分别两种,间接激活和直接激活p53,一种是通过靶向抑制p53活性的蛋白如诺华的p53-Hdm2抑制剂、NexusPharma的p53-Mdm2抑制剂等,另一种是直接靶向p53蛋白如Aprea Therapeutics的APR-246、Cotinga Pharmaceuticals的COTI-2等。下面重点介绍下3种处于临床阶段的靶向p53蛋白小分子药物。
Aprea Therapeutics的APR-246是一款靶向泛p53突变的小分子,临床上对超过70多种p53突变类型肿瘤患者都有效果。最早在2009年进入临床试验(NCT00900614),目前仍有7项临床试验正在进行,其中有一项是3期临床试验。资格认定方面,FDA授予BTD、ODD、FTD治疗MDS;EMA授予ODD治疗MDS、AML和卵巢癌,预计2021年NDA,也就是整个临床阶段到上市跨度大约12年。(来源:资料1)
Cotinga Pharmaceuticals的COTI-2是一款靶向泛p53突变的小分子,从2015年开始进入临床试验,处于1期阶段,资格认定方面,FDA授予ODD治疗卵巢癌。(来源:资料2)
Innovation Pharmaceuticals的Kevetrin是一款靶向泛p53突变的小分子,从2012年开始进入临床试验,处于2期阶段,资格认定方面,FDA授予ODD治疗卵巢癌、前列腺癌和视网膜母细胞瘤以及RPDD治疗儿童视网膜母细胞瘤。(来源:资料3)
不难看出,即使是针对肿瘤中突变频率最高的p53蛋白小分子激活剂,从临床推进到上市至少需要12年时间,时间偏长,除了与靶向突变p53蛋白的难度偏高之外,很大部分原因在于临床策略上,基本按照常规模式,广泛入组p53突变的各瘤种患者,找出效果较好的瘤种,再扩大规模,很显然,这种策略对于p53激活剂来说收效甚微,因为p53突变类型有很多,入组的患者不一定是该药最适合的患者。
在美国,大约有75%的肿瘤科医生使用基因测序,正是由于近几年基因测序逐渐普遍起来,精准医学越来越受到重视,出现了三款“不限瘤种”的广谱抗癌药,抗PD-1抗体派姆单抗(Pembrolizumab/Keytruda)治疗MSI-high/dMMR肿瘤,拉罗替尼和恩曲替尼治疗NTRK基因融合肿瘤。下面先回顾下这三款广谱抗癌药的上市历程。
派姆单抗(Pembrolizumab/Keytruda)最早于2014年被批准用于黑色素瘤,在2017年5月的时候获批用于治疗MSI-high/dMMR肿瘤,正式成为“不限瘤种”的广谱抗癌药,这个新适应症的批准是基于肿瘤缓解率和DOR,4个临床试验(1期/2期临床),共149名患者,时间跨度从2013年到2017年,从临床到上市用时4年。(来源:资料4、5、6)
拉罗替尼于2018年被批准用于治疗NTRK基因融合实体瘤,成为第二款“不限瘤种”的广谱抗癌药,这个适应症的批准是基于ORR和DOR,3个临床试验(1期/2期临床),共55名患者,时间跨度从2014年到2018年,从临床到上市用时4年半。(来源:资料7、8)这款药的销售额峰值预测8.5亿美元。(来源:资料9)
恩曲替尼于2019年被批准用于治疗NTRK基因融合实体瘤,成为第三款“不限瘤种”的广谱抗癌药,这个适应症的批准是基于4个临床试验(1期/2期临床),有效性数据来源于54名患者,安全性数据来源于355名患者,时间跨度从2012年到2019年,从临床到上市用时7年。(来源:资料10、11)这款药的销售额峰值预测7亿美元。(来源:资料12)
可以发现,这三款广谱抗癌药的适应症批准都是没经过3期临床试验的,从临床到适应症获批大概5年左右,这就是基因测序所带来的精准医学的优势,让药物能够快速匹配到适合人群,快速上市。这将是化学药物当中,继PROTAC后又一个新风口,泛瘤种基因驱动的靶向药。
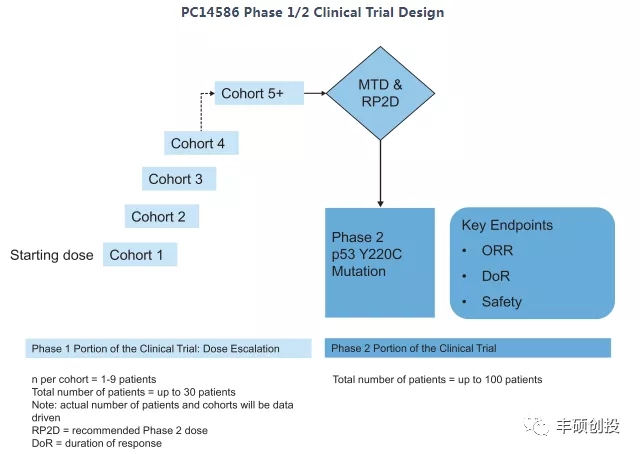
充分考虑到这些成功经历,PMV Pharma公司的PC14586临床推进策略就是仿照他们,直接进行1/2期临床试验,入组p53 Y220C突变的泛瘤种患者,结果出来后就敢向FDA提出NDA,想成为第四款广谱抗癌药,见下图。
图2 PC14586临床计划(来源:PMVP招股说明书)
简单估算下,根据拉罗替尼和恩曲替尼的销售额峰值预测数值可以反推到粗略计算公式,即全球实体瘤市场规模×该基因频率,按照这个公式我们粗略算到靶向p53 Y220C突变的PC14586未来销售额峰值为8亿美元左右。
参考资料
1.https://ir.aprea.com/static-files/27fe55aa-4eca-492f-b268-561d55b8bc0c
2.https://www.pharmaceuticalonline.com/doc/fda-grants-orphan-drug-status-to-coti-s-ovarian-cancer-drug-coti-0001
3.http://www.ipharminc.com/kevetrin-1
4.https://www.accessdata.fda.gov/drugsatfda_docs/appletter/2014/125514Orig1s000ltr.pdf
5.https://www.accessdata.fda.gov/drugsatfda_docs/appletter/2017/125514Orig1s014ltr.pdf
6.https://www.accessdata.fda.gov/drugsatfda_docs/nda/2019/125514Orig1s014.pdf
7.https://www.accessdata.fda.gov/drugsatfda_docs/appletter/2018/211710Orig1s000ltr.pdf
8.https://www.accessdata.fda.gov/drugsatfda_docs/nda/2018/210861Orig1s000_211710Orig1s000MultidisciplineR.pdf
9.https://www.fiercebiotech.com/special-report/50-vitrakvi
10.https://www.accessdata.fda.gov/drugsatfda_docs/appletter/2019/212725Orig1s000ltr.pdf
11.https://www.accessdata.fda.gov/drugsatfda_docs/nda/2019/212725Orig1s000,%20212726Orig1s000MultidisciplineR.pdf
12.https://www.fiercebiotech.com/special-report/20-rozlytrek
扫描上面二维码在移动端打开阅读