【拷贝数变化用于通过寻找在 DNA 中扩增或缺失基因的重复模式来分析多种癌症类型中的肿瘤】已知较少的侵袭性的癌症具有完整的基因组 - 细胞中的全套基因 - 而更具侵袭性的癌症的基因组倾向于具有大量异常基因。现在,肿瘤细胞中 DNA 模式的新的研究表明,这些异常的遗传特征不是随机的,而是反映肿瘤进化中的选择性。研究结果还表明,这些变化驱动细胞中的葡萄糖代谢,这提高了肿瘤的适应性,并可以加速癌症生长。
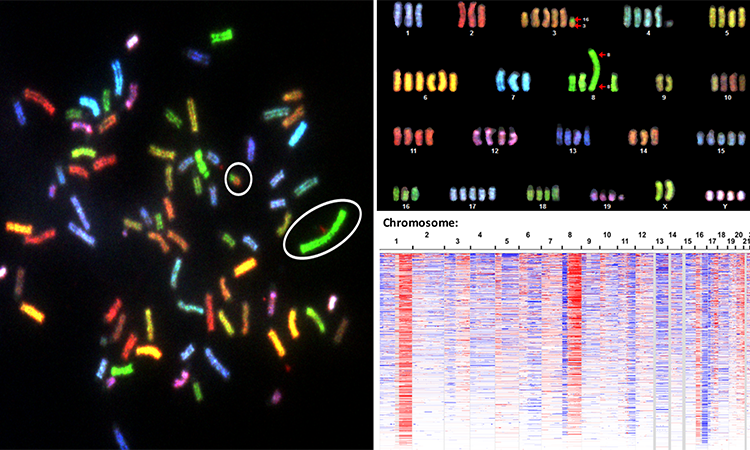
这项新研究由高级作者 Thomas Graeber 博士领导。第一作者是 USC 维特比工程学院化学工程助理教授 Nicholas Graham 博士和 UCLA Crump 分子成像研究所博士后研究员 Aspram Minasyan 博士。
拷贝数变化(CNA)测量用于通过寻找在 DNA 中扩增或缺失基因的重复模式来分析多种癌症类型中的肿瘤。现代研究主要集中于个体癌症基因作为 DNA 突变和拷贝数变化的主要靶标,特别是癌基因和肿瘤抑制基因。然而,科学家继续观察肿瘤中的许多复发性 CNA 模式,这些模式不能由这些典型癌症基因充分解释。
长期以来已知健康细胞和肿瘤形成细胞之间的根本区别是重编程的细胞代谢。改变的代谢以许多方式有益于细胞转化,特别是在将葡萄糖转化为能量的能力方面。这个过程称为糖酵解,可以燃烧肿瘤生长,也用于通过 PET 成像检测肿瘤。研究进一步显示较高水平的糖酵解活性和最具侵袭性的癌症之间强相关。
在五年的研究中,Graeber 和他的同事使用了来自人类肿瘤,癌细胞系和小鼠癌症模型的 CNA 数据的交叉分析。该团队分析了 15 种不同癌症类型的样品。他们发现 DNA 扩增和缺失的 CNA 模式预示增加的糖酵解活性和肿瘤细胞的快速生长。为了了解酶如何在这个过程中发挥作用,科学家们比较了人类肿瘤和小鼠模型的 CNA 模式。他们发现了 26 个具有一致基因改变的 DNA 区域,其中包含糖酵解途径中的 11 种酶以及已知的癌症驱动基因。
研究人员接着使用实验性永生化系统和基因工程来直接证明糖酵解酶可影响 CNA 标签。通过在不同时间点对细胞进行取样,研究人员能够显示这些模式如何演变,从而塑造癌症基因组。
该研究是第一个使用高分辨率全基因组 CNA 标记来鉴定和定义新类型的肿瘤的研究之一。有了这些发现,研究人员可以建立改进的癌症模型,并推进治疗所有类型的疾病的发展。
扫描上面二维码在移动端打开阅读





