广州生物院揭示疟原虫感染小鼠血浆外泌体抑制肿瘤血管生成的分子机制
6 月 26 日,自然出版集团系列期刊 Oncogensis 在线发表了中国科学院广州生物医药与健康研究院陈小平课题组的最新研究成果 Exosomes from Plasmodium-infected hosts inhibit tumor angiogenesis in a murine Lewis lung cancer model。该研究首次发现疟原虫感染小鼠血浆外泌体(exosomes)能够抑制肿瘤血管生成,并初步阐明其分子机制。该研究加深了对疟原虫感染宿主所分泌的外泌体与肿瘤血管生成之间的相互作用的认识,为开发疟原虫感染来源的外泌体作为一种新型抗肿瘤制剂奠定了基础。该成果是博士研究生杨一峻等在研究员陈小平等指导下完成的。
外泌体是细胞外膜泡,在细胞与细胞间通讯中起作用。在病原体感染宿主时,外泌体也发挥重要作用。但是,在上述论文发表之前,科学家们并不清楚疟原虫感染宿主所产生的外泌体是否能够抑制肿瘤血管生成,更不知道其中的分子机制。
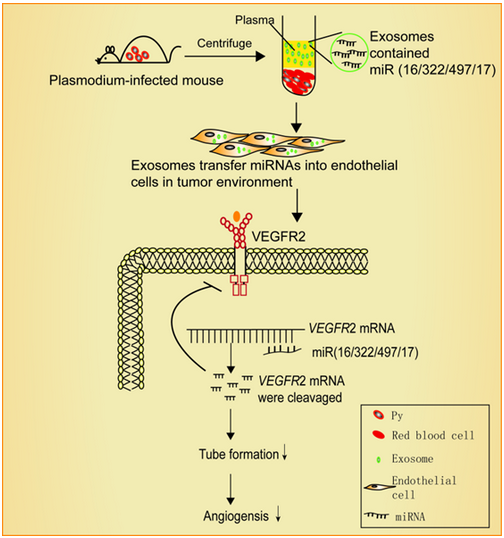
研究人员选用肺癌小鼠模型作为研究对象,从感染疟原虫的小鼠血浆中获得外泌体,并将这些外泌体注射到小鼠的肿瘤内部,并与没有疟原虫感染的小鼠血浆外泌体进行对照。研究发现,疟原虫感染小鼠的血浆外泌体显著抑制肿瘤血管的生成。进一步的研究发现,疟原虫感染的小鼠血浆外泌体通过至少四种特殊的微小 RNA(miR16-5p/17-5p/322-5p/497-5p)抑制血管内皮细胞 VEGF 受体(VEGFR2)的表达从而阻断血管生成的信号通路。这些发现加深了人们对疟原虫抗癌机理的理解,并为疟原虫疗法治疗癌症的临床研究提供进一步的理论依据。
该项目得到了国家自然科学基金、科技部重点科技计划、广东省及广州市科技计划等的支持。
http://www.nature.com/oncsis/journal/v6/n6/full/oncsis201752a.html
扫描上面二维码在移动端打开阅读





