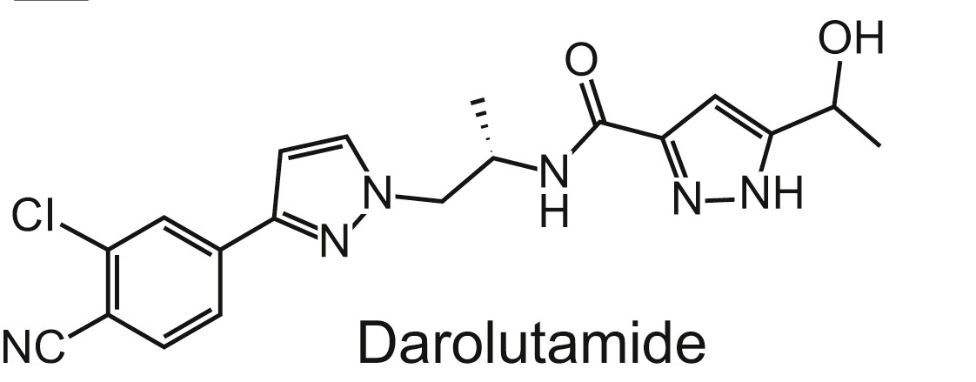
药品概述
2019年7月30日,美国食品和药物管理局(FDA)批准新型抗癌口服片剂Nubeqa(darolutamide 达洛鲁胺)口服片剂上市,用于非转移性去势抵抗性前列腺癌(nmCRPC)患者的治疗。
Darolutamide于2020年3月在欧盟获得批准,商品名为Nubeqa®,用于治疗具有高风险进展为转移性疾病的患有非转移性去势抵抗性前列腺癌(nmCRPC)的男性患者。
2021年2月2日,NMPA 批准达罗他胺(Darolutamide)用于治疗非转移性去势抵抗性前列腺癌(nmCRPC)。
2022年8月,达罗他胺(Darolutamide)获美国FDA批准治疗转移性激素敏感性前列腺癌 (mHSPC) 。
Darolutamide是一种雄激素受体抑制剂(ARi),其独特的化学结构与受体结合具有很高的亲和力,展现出很强的拮抗活性,从而抑制受体功能和前列腺癌细胞的生长。该化合物也正在一项III期ARASENS试验中用于转移性激素敏感性前列腺癌的研究。
2021年12月3日,中国国家医保局发布了2021年《国家基本医疗保险、工伤保险和生育保险药品目录(2021年)》(以下简称“国家医保目录“)。达罗他胺进入新版医保目录。
医保内适应症范围
治疗有高危转移风险的NM-CRPC成年患者。
2023年3月15日,药监局官网显示,拜耳口服雄激素受体抑制剂达罗他胺(darolutamide, Nubeqa)新适应症上市申请获得批准。本次获批的适应症为联合多西他赛用于治疗转移性激素敏感性前列腺癌 (mHSPC) 患者。
简要说明书
| Darolutamide 达罗他胺 (诺倍戈,Nubeqa) 说明书 | |
| 药物: | 达罗他胺片 Darolutamide(诺倍戈,Nubeqa) |
| 中国上市情况: | 已上市 |
| 靶点: | AR |
| 治疗: | 治疗非转移性去势抵抗性前列腺癌患者。 |
| 参考用法用量: | 推荐剂量为600mg(两片300mg薄膜衣片),每日两次,口服,相当于日总剂量为1200 mg。 |
| 不良反应: | 见说明书。 |