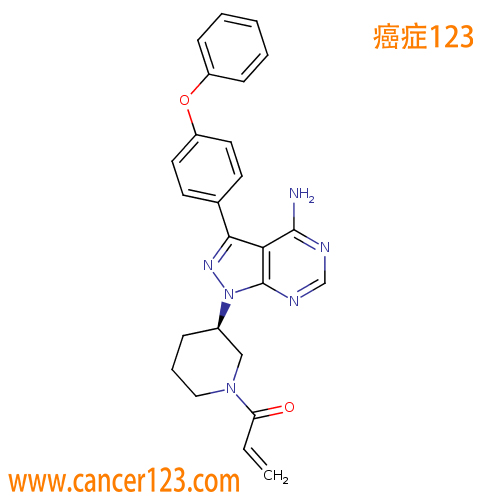
药品概述
伊布替尼是第一种布鲁顿酪氨酸激酶(BTK)抑制剂,可以与BTK活性位点中心形成共价键,从而抑制BTK活性。2013年11月13日获FDA批准上市。
在美国,伊布替尼(Ibrutinib,依鲁替尼)迄今已收获FDA批准的7个适应症。
2013年11月,FDA批准伊布替尼用于治疗前期接受过至少一次来那度胺或者其他药物治疗的套细胞淋巴瘤(MCL)患者。
2014年2月,FDA批准伊布替尼用于既往接受过至少一次治疗的慢性淋巴细胞白血病(CLL)患者的治疗。
2014年7月,FDA批准伊布替尼用于治疗携带del 17p删除突变的慢性淋巴细胞白血病(CLL)患者。
2015年1月,FDA批准伊布替尼用于治疗华氏巨球蛋白血症 (WM),这是一种始于人体免疫系统的罕见癌症。这款药物用于这一疾病获得了突破性治疗药物资格。
2016年3月,FDA批准伊布替尼用于慢性淋巴细胞白血病(CLL)患者的一线治疗。此次批准,首次为CLL群体提供了一种无化疗(chemotherapy-free)的一线治疗选择。
2016年5月,FDA批准伊布替尼作为单药或联合苯达莫司汀+利妥昔单抗(BR)用于治疗伴有或不伴有染色体17p删除突变(del 17p)的小淋巴细胞性淋巴瘤(SLL)患者。
2017年8月,FD批准伊布替尼治疗患有慢性移植物抗宿主病(cGVHD),且先前的治疗已遭失败的成人患者。这是美国FDA批准的治疗这一疾病的首款疗法。
2018年2月,FDA授予伊布替尼治疗胃癌(包括胃食管连接腺癌)的孤儿药资格。而依鲁替尼开发进度最快的实体瘤适应症是胰腺癌(Ⅲ期)。
伊布替尼(亿珂)在中国获批的适应症
在2017年8月30日经国家食品药品监督管理总局批准单药适用于既往至少接受过一种治疗的慢性淋巴细胞白血病/小林吧细胞淋巴瘤以及既往至少接收过一种治疗的套细胞淋巴瘤患者的治疗。
2018年11月23日强生公司在华制药子公司西安杨森制药有限公司宣布,旗下亿珂(伊布替尼胶囊)新适应症获国家药品监督管理局批准,可单药用于既往至少接受过一种治疗的华氏巨球蛋白血症(WM)患者的治疗,或者不适合接受化学免疫治疗的患者的一线治疗;与利妥昔单抗联用,用于华氏巨球蛋白血症患者的治疗。
简要说明书
| 伊布替尼Ibrutinib(Imbruvica 亿珂®)说明书 | |
| 药物: | 伊布替尼Ibrutinib |
| 中国上市情况: | 已上市 |
| 靶点: | BTK |
| 治疗: |
1.单药适用于既往至少接受过一种治疗的套细胞淋巴瘤患者的治疗。 |
| 参考用法用量: | 治疗 MCL 的推荐剂量为 560mg(4 粒 140mg 的胶囊),每日一次;治疗CLL/SLL 的推荐剂量为 420mg(3 粒 140mg 的胶囊),每日一次。 |
| 不良反应: | 出血,感染,血细胞减少,间质性肺疾病,房颤,白细胞淤滞,高血压,继发恶性肿瘤,肿瘤溶解综合征 |