免疫检查点抑制剂治疗开创了治疗新时代,随之的疗效预测评价的生物学标记物研究也将带来更大的益处。
引言
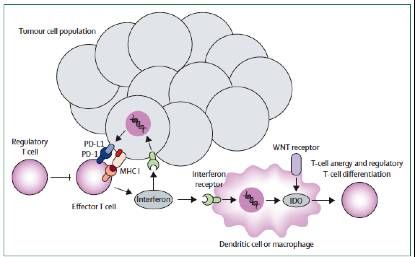
免疫系统对肿瘤细胞监视和清除有重要作用。肿瘤细胞通过各种机制逃避免疫是肿瘤特征之一。Chen和Mellman描述的肿瘤免疫循环是抗肿瘤免疫增强反应策略的基石。包括的步骤有:肿瘤抗原的释放、树突状细胞(DC)呈递、外周免疫细胞的启动和活化、T细胞侵润至肿瘤间隙、肿瘤细胞识别和免疫调节细胞死亡。外周免疫细胞的启动和活化的过程形成了所谓的T细胞炎症表型。耐受机制普遍存在,如对干扰素γ刺激下PD-L1和IDO上调,其降低了经免疫调节的肿瘤清除能力。(图). 免疫治疗被认为是有T细胞炎症表型患者最有效的治疗策略。高剂量的白介素-2和过继免疫T细胞输注对晚期肿瘤患者可达到持续的临床获益。目前焦点聚集到免疫检查点的靶向调控。CTLA-4抗体ipilimumab在两项3期随机试验中表明提高晚期黑色素瘤总生存,成为第一个批准的检查点抑制剂。但ipilimumab单药治疗的客观反应低,荟萃分析ipilimumab 研究,22%的晚期黑色素瘤治疗后至少生存3年。抗PD-1药物pembrolizumab和nivolumab经美国FDA批准用于晚期不能切除的黑色素瘤和非小细胞肺癌。Pembrolizumab或nivolumab一线治疗黑色素瘤的客观反应率为40-45%,化疗失败的NSCLC则为20%。
Nivolumab还被FDA批准用于转移性肾癌、难治性霍奇金淋巴瘤;抗PD-L1药物atezolizumab用于晚期膀胱癌。还有一些抗PD-1和PD-L1的药物在一系列的实体瘤和血液恶性肿瘤中展现出有前景的临床活性,如抗PD-L1抗体durvalumab和avelumab。
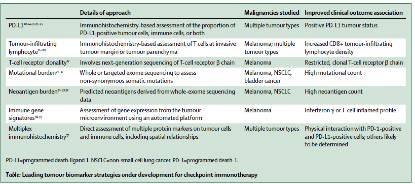
尽管如此,免疫相关的不良事件(immune-related adverse events)如皮炎、大肠炎和肝炎随着联合检查点阻断剂的使用,风险也相应增加。建立检查点免疫治疗预测性生物标记物对增加治疗获益显得至关重要。需要一个或多个有很高阳性和阴性预测价值的生物学标记物来帮助肿瘤医生作出治疗策略。建立预测性生物标记物对更有侵袭性的治疗至关重要,如nivolumab和ipilimumab联合治疗。如严重但可控的风险和有总反应的患者比例一样高。生物标记物可以用于单药和联合免疫治疗间的患者进行分层,什么样的免疫治疗优先给予(一线还会挽救),同时预测什么样的患者可能对检查点免疫抑制治疗无效,从而避免不必要的毒性。目前,多种生物标记物关注的是鉴别T细胞炎症表型和所谓的tumour foreignness ,(如突变负荷、新抗原),它们作为抗CTLA-4和抗PD-1或抗PD-L1治疗临床疗效相关的评价指标。本综述研究生物标记物的进程,以帮助抗肿瘤的检查点抑制剂免疫治疗的实施。 (table).
PD-L1 表达
直接检测肿瘤细胞上PD-L1的表达是预测抗PD-1或抗PD-L1治疗反应的合理的生物学标志物。从黑色素瘤、非小细胞肺癌、肾癌、前列腺癌等nivolumab 药物的1期研究上看,用免疫组化方法检测肿瘤活检标本PD-L1的表达,界定肿瘤细胞PD-L1阳性的阈值为5%,25例中有9例(36%)PD-L1阳性的患者对nivolumab,有客观反应,而阴性的患者无一例有反应。随后的研究也证实这点。无进展生存(PFS)和总生存(OS)在晚期黑色素瘤和NSCLC上,也是PD-L1阳性比阴性的患者在nivolumab治疗后要长。PD-L1免疫组化诊断试剂盒也经FDA批准用于晚期NSCLC和膀胱癌患者,但是PD-L1阳性只是pembrolizumab用于治疗NSCLC的唯一条件。但是免疫组化PD-L1阴性的患者在抗PD-1或抗PD-L1治疗后仍然有临床获益。实际上,PD-L1阴性的肿瘤患者也有客观反应,从11%至20%不等,CheckMate 067黑色素瘤试验中,nivolumab单药治疗的总反应率达到41%,nivolumab加ipilimumab为54%,这些数据提示抗PD-1或抗PD-L1治疗的阴性预测价值不理想,nivolumab,只有58%,nivolumab加ipilimumab为45%。
PD-L1免疫组化作为抗PD-1或抗PD-L1治疗生物学标记物的不可靠性是多因素所致。第一,PD-L1表达受多种机制调控,包括MAPK和PI3K或Akt通路、转录因子HIF1、STAT3和NFkB,以及外显因素。它还可以由肿瘤微环境中的其他免疫细胞表达。除了PD-L1基因(CD274)拷贝数可以如霍奇金淋巴瘤样导致表达,而且表达是暂时性的,在患者间和肿瘤间的表达有异质性。因此某一时间节点或某一肿瘤部位或肿瘤某一部分并不能准确反应患者PD-1或PD-L1轴的真实情况。第二个重要因素PD-L1免疫组化抗体的不均一性和正在使用的PD-L1阳性阈值不统一。不同试验中使用的抗体不一样。PD-L1表达阈值有差别,有的定为1%或以上,有的用50%或以上。没有一项研究报道哪个阈值的阳性和阴性预测值可达到100%。另一个重要方面是单一PD-L1免疫组化没有将阻碍抗PD-1或抗PD-L1治疗反应的因素考虑进来,如肿瘤微环境中是否有活化的免疫细胞影响PD-1或PD-L1轴,或其他伴随抑制性免疫通路(如IDO、FoxP3+调节性T细胞和淋巴活化基因3[LAG3])
尽管有这么多不足,PD-L1免疫组化在抗PD-1或抗PD-L1治疗中,区分患者发挥了重要作用。确保PD-L1阳性肿瘤实验组和对照组患者均匀分布,对避免因生物学差异导致的偏倚是必要的。在有多种治疗方法可供选择时,PD-L1表达可以指导治疗。比如pembrolizumab 治疗晚期NSCLC的1期研究(KEYNOTE-001)表明PD-L1阳性的肿瘤(免疫组化定义为≥50%肿瘤细胞)客观反应率为45%,而阴性的患者(免疫组化定义为<1%肿瘤细胞)为11%。NSCLC患者中,PD-L1阴性也可以从替代治疗途径中获益,如化疗或不同的免疫治疗。这种观点也得到了CheckMate 057试验的证实。该试验比较的是二线nivolumab VS多西他赛治疗非角化NSCLC,对于PD-L1阴性的患者,在多西他赛治疗后,可以获得更长的PFS和相似的OS。在CheckMate 067试验的原始数据基础上得出结论,建议PD-L1阳性作为选择抗PD-1抗体,而不是nivolumab加ipilimumab联合治疗的生物学标记物。但是最新的数据显示nivolumab加ipilimumab比单药nivolumab治疗PD-L1阳性的黑色素瘤有更长的PFS。基于此,单一的PD-L1免疫组化还不能完全作为决定抗PD-1还是抗PD-L1治疗策略、确定哪些患者可以从单药VS抗PD-1或抗PD-L1联合治疗有相同获益,临床上常规使用的生物学标记物。
肿瘤侵润淋巴细胞
在对结直肠癌、黑色素瘤和NSCLC的回顾性研究中发现,肿瘤活检标本中的淋巴细胞侵润与延长生存有关。实体肿瘤,如结直肠癌、黑色素瘤转移灶中出现异位淋巴结样结构,可以更好地预测生存。如有数据显示3期NSCLC患者中,治疗前活检标本CD8+肿瘤侵润淋巴细胞密度高的比低的患者,有更长的PFS和OS。免疫识别肿瘤细胞可以导致宿主免疫反应或T细胞炎性肿瘤表型,可以通过免疫机制提高疾病控制,因此可以作为预后预测的生物学指标。T细胞炎性肿瘤微环境的存在可以令患者从MAGE-A3 疫苗和大剂量的白介素2中获益。因此基线肿瘤侵润淋巴细胞可以作为检查点抑制剂免疫治疗的预测性生物学标志物。
在ipilimumab 治疗转移性黑色素瘤的2期研究中,基线的肿瘤侵润淋巴细胞与临床疗效(CR、PR、持续超过24周的SD)无关。然而在第二剂的ipilimumab 使用后获得的肿瘤活检标本中肿瘤侵润淋巴细胞密度增加比无增加的患者有更显着更大的临床反应。KEYNOTE-001 研究分析黑色素瘤患者中肿瘤侵润淋巴细胞与pembrolizumab 治疗反应的关联。在肿瘤实质和和肿瘤边缘,定量检测肿瘤侵润淋巴细胞密度。治疗有反应患者治疗前肿瘤标本中CD8+(不是CD4+)T细胞密度比进展的患者要高。与ipilimumab观察到的现象类似,在抗PD-1治疗有反应组,肿瘤中CD8+T细胞密度要高,但在进展组却相反。另一项予抗PD-1治疗的黑色素瘤研究显示,治疗前标本中的CD8+、CD3+和CD45RO+T细胞密度与治疗反应有中度关联。在抗PD-1治疗后,关联更加显着。但是要看到,有反应者和进展者的基线CD8+T细胞密度有重叠,这就不利于确定临床有意义的预测性生物标记物的绝对阈值。
T-细胞受体克隆性
Tumeh等人研究基线肿瘤侵润淋巴细胞是否有参与肿瘤特异免疫反应比较少的T细胞受体簇,以及是否这种狭窄的受体簇与对pembrolizumab 的反应有关。新一代测序检测治疗前黑色素瘤细胞上所有独特的、可变T细胞受体β链区重排。T细胞受体β链发挥作用在反应组比进展组有更多的限制性(更多克隆形成,较少多样性)。治疗前和治疗后的穿刺样本显示反应组在抗PD-1治疗后,比进展组在克隆上有10倍的增加,这就提示有治疗后肿瘤特异反应。基线肿瘤受体克隆与肿瘤侵润淋巴细胞密度没有高度相关,意味着某些肿瘤侵润淋巴细胞低密度的患者,如果肿瘤侵润淋巴细胞有对肿瘤抗原特异的限制性T细胞受体克隆,仍然可以获益于抗PD-1治疗,但这一假设仍然需要在更多患者中去验证。
突变或新抗原负荷
临床前研究发现肿瘤旁路基因的体细胞突变产生的新抗原可以作为抗肿瘤继发免疫反应(antitumour adaptive immune responses)的初始驱动因素。
Rooney 等人的研究显示,以肿瘤内穿孔素1和颗粒酶B基因表达衡量的免疫细胞溶解活性与更高的突变数有关。他们预测在一系列实体肿瘤中有抗基因的新表型。他们的发现支持这样以观点:有高突变负荷的肿瘤类型对免疫治疗有更好的反应。黑色素瘤和肺癌是被认为有最多新抗原的肿瘤,对检查点免疫治疗的反应也会更好。在对结直肠癌的2期pembrolizumab研究中发现,错配修复缺陷(比错配修复好的,有>20倍以上的突变负荷)与错配修复好的比较,突变负荷和新抗原在免疫活性中发挥了作用。最新的数据也表明,错配修复缺陷比错配修复好的患者,在晚期结直肠癌中,有更高的客观反应率(50% VS 0%)。PFS和OS也更长。运用突变或新抗原负荷也作为检查点抑制剂免疫治疗预测性生物学指标。
外周血标记物
检测外周血标记物是接受免疫检查点治疗的一个方便、无创的生物学标记物。目前还没有前瞻性研究证实预测性生物指标的意义。在ipilimumab的研究中,发现低中性粒细胞计数(<7500 细胞/μL) 、低中性粒/淋巴细胞比(<3)、低绝对单核细胞计数(<650 细胞/μL)、低骨髓来源抑制细胞(MDSC)(<5.1%)、高FoxP3+调节T细胞(≥1.5%)、高淋巴细胞(≥10.5%)、高嗜酸性粒细胞(≥50 细胞/μL )与更长的OS和PFS有关。治疗前后的动态变化也与ipilimumab 治疗的黑色素瘤临床获益有关。增加的T细胞受体基因多样性(如含有许多V-J重排受体簇)和均一性(频率均一分布)与临床获益显着相关。但可能因样本量小,在总生存上无相关性。
免疫基因印迹
通过肿瘤微环境中基因表达谱以更加广的评价活跃的固有和获得性免疫也许可以有效预测检查点抑制剂治疗的临床获益。回顾性分析ipilimumab治疗晚期黑色素瘤的2期临床试验(CA184004)证明基因表达谱可以作为有用的预测性生物学标志物。这项研究中,提取总的RNA,分析50例治疗前肿瘤活检标本。患者ipilimumab治疗后的临床疗效分为客观反应、稳定状态延长和无临床疗效。组间基因通路分析有很大不同。22个免疫相关基因有至少2.5倍以上的增加,包括细胞毒T细胞标记物(如CD8A、颗粒酶B和穿孔素1)、Th1细胞因子或趋化因子、MHC II类(HLA-DQA1)和其他免疫相关基因(如NKG7, IDO1)。更大的治疗前和治疗后表达值(如CXCL11、CXCR3)与总生存延长相关。
免疫基因印迹,尤其是γ干扰素诱导的,可能是预测抗PD-1或抗PD-L1治疗临床获益的很好的生物标记物。这一理论得到Johnson 等人研究数据的支持:MHC II (HLA-DR)的高表达与临床反应增加有关,黑色素瘤患者在抗PD-1或抗PD-L1治疗后PFS和OS比MHC II (HLA-DR)低表达者延长。Ribas 等人的数据也表明了在晚期黑色素瘤患者中有干扰素炎症免疫基因印迹与治疗反应的相关性。通过ROC曲线,可以制定干扰素-γ评分阈值,有反应者的阳性预测值为59%,无反应者的阴性预测值达到90%。
多重免疫组化
运用多重免疫组化技术直接评价肿瘤和免疫细胞表型以及它们在空间上的关联可以提供直接的有关肿瘤微环境中免疫状态的相关信息,这优于或者说是基因表达谱的补充。目前的方法可以用标准的荧光显微镜作到四色和五色荧光染色(或者用多光谱的照相机作到8色)。对临床应用有最大帮助。例如:多光谱的免疫组化分析黑色素瘤肿瘤切片上的CD3、CD8、FoxP3、CD163和PD-L1表达以预测哪些患者可以在过继细胞治疗后能成功产生肿瘤侵润淋巴细胞。CD8+T细胞与CD3+FoxP3+调节T细胞的比值与肿瘤侵润淋巴细胞的生长呈强相关。
联合生物学标记物方法
将两个或以上的评价肿瘤微环境免疫状态的方法结合起来可以作为预测免疫检查点抑制剂疗效的复合预测性生物学标记物。当肿瘤侵润淋巴细胞计数低时,肿瘤PD-L1可以高表达,而肿瘤侵润淋巴细胞密度高时,可以不表达PD-L1。单一指标评价可能会有错误的结论。相似的,不是所有的高突变或新抗原负荷可以显示出治疗前免疫状态。基因表达谱如干扰素γ评分,结合多种免疫变量可以准确预测免疫治疗的反应者和无反应者。PD-L1的mRNA浓度不如免疫组化可靠。但免疫组化也有局限性。联合标记物的优势已经在2016年ASCO年会和2015年欧洲肿瘤大会上得到数据的支持。
小结
以检查点抑制剂为基础的免疫治疗将抗癌治疗带入了令人激动人心的时代。黑色素瘤和其他肿瘤因此得到了持续反应。尽管PD-1或PD-L1的单一药物治疗有很好的耐受性,但随着联合治疗的运用,免疫相关的不良事件的风险也随之增加。因此需要不断发现预测性生物学标记物,以令患者获益最大化、减小毒性风险,以及规范联合治疗。最关注的地方是肿瘤细胞上的PD-L1表达。虽然在有临床获益的患者上,PD-L1阳性的表达较强,对多数肿瘤而言,单单检测PD-L1对患者选择是不够的。我们在这篇综述中讨论了PD-L1检测的现状,探索肿瘤侵润淋巴细胞、突变负荷、免疫基因印迹和多重免疫组化下,有关新免疫标记物方法的最新数据。未来对以检查点抑制剂为基础的免疫治疗进行有效预测的生物学标记物的研究,会将肿瘤免疫微环境的最佳特征的多种研究途径整合进来。
(生物谷Bioon.com)
相关会议推荐

2017”肿瘤免疫+”研讨会
会议时间:2017.3.10 -3.11 会议地点:上海
会议详情: http://www.bioon.com/z/2017tumor/
扫描上面二维码在移动端打开阅读