为了与周围微环境进行联系,肿瘤细胞会主动释放大量的胞外囊泡(EVs),包括外泌体、微泡(MV)或微粒、以及凋亡小体。这些由肿瘤释放的 EV,在肿瘤患者的体液中是非常丰富的,它们在促进肿瘤生长和进展中起到了关键作用。例如,NCI-H460 肿瘤细胞系释放含有 EMMPRIN(一种在肿瘤细胞内高表达的跨膜糖蛋白)的 MV,MV 包裹的 EMMPRIN 通过促进成纤维细胞中的基质金属蛋白酶的表达,从而促进肿瘤细胞的侵袭和转移。肿瘤细胞外泌体还可以递送有活性的 Wnt 蛋白以调节靶细胞 b -catenin 相关的基因表达。肿瘤细胞释放含有 P - 选择素糖蛋白配体 1(P-selectin glycoprotein ligand 1 )的微粒会加速体内血栓的形成,这样通过靶向 P - 选择蛋白糖蛋白配体 1,研究人员就能够预防血栓的形成。虽然这些研究有阻止肿瘤细胞转移潜力,但是肿瘤细胞有活性的外泌体是如何被分泌的机制仍然不清楚。之前的研究表明在肿瘤发生期间外泌体的活性会增加,但是在此过程中肿瘤细胞进行胞吐过程的分子机制需要进一步阐明。
1 月 9 日,Nature Communications 杂志发表了来自南京大学张辰宇、曾科课题组、南京中医药大学胡刚课题组以及美国佐治亚州立大学 Yuan Liu 课题组的研究成果,他们发现,丙酮酸激酶 M2 型(PKM2)——肿瘤细胞进行无氧糖酵解(被称为 Warburg 效应)的关键酶,在促进外泌体从肿瘤细胞的释放的过程中发挥关键作用。研究人员发现,磷酸化突触体相关蛋白 23(SNAP-23)在肿瘤细胞中是 PKM2 的磷酸化底物,调控分泌颗粒或包含外泌体的多泡体的停留和释放。在外泌体分泌期间,磷酸化的 PKM2 会形成具有低丙酮酸激酶活性和高蛋白激酶活性的二聚体结构,然后与细胞膜附近的 SNAP-23 结合,导致 SNAP-23 的 95 位丝氨酸(Ser95)的磷酸化和肿瘤细胞外泌体释放的上调。SNAP-23 的磷酸化突变体(Ser95 突变为 Ala95)的表达会显着减少 PKM2 介导的外泌体释放,而 SNAP-23 磷酸化模拟体(Ser95 突变为 Glu95)的表达会 rescue 由 PKM2 敲低造成的低水平外泌体的释放量。由此研究人员得出结论,PKM2 的磷酸化和二聚体化,不仅可以转换肿瘤细胞代谢从氧化磷酸化到无氧糖酵解,还可以通过直接磷酸化 SNAP 23 促进肿瘤细胞外泌体的分泌。
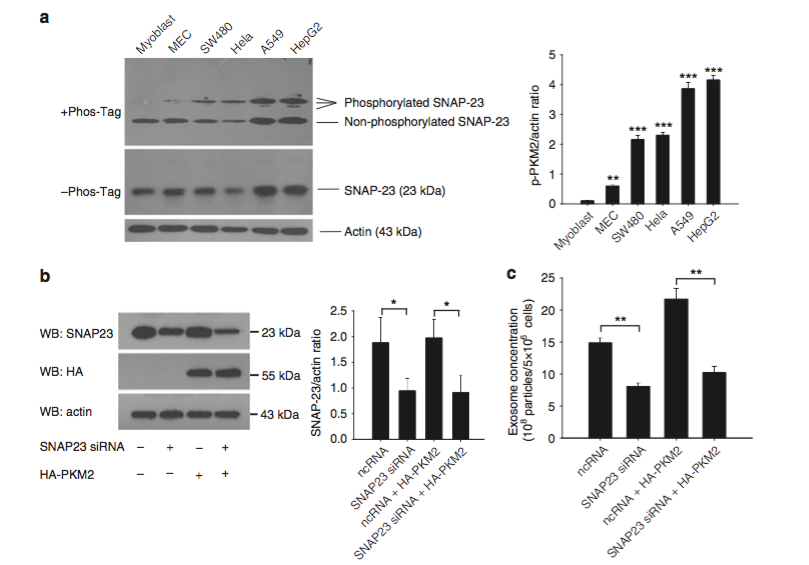
图 1:PKM2 通过 SNAP23 促进外泌体的释放
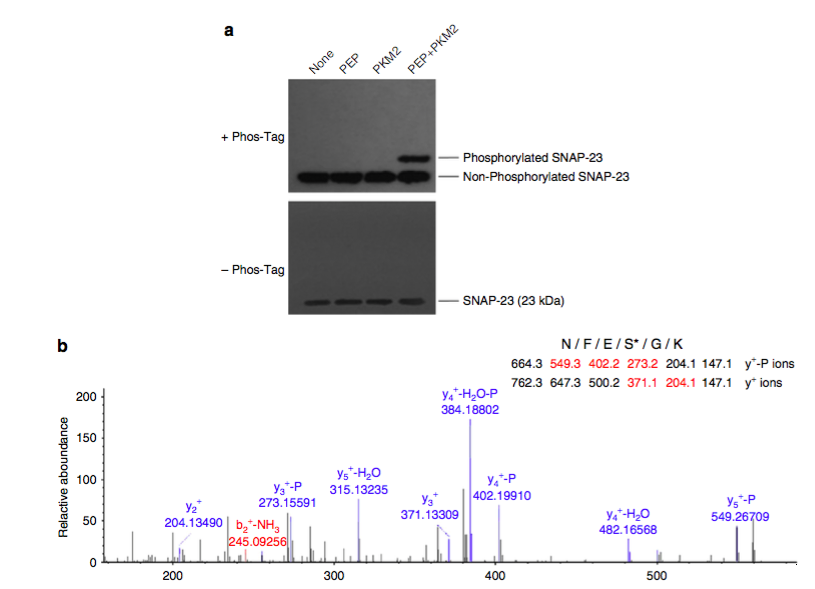
图 2:PKM2 直接磷酸化 SNAP23 的 95 位丝氨酸位点
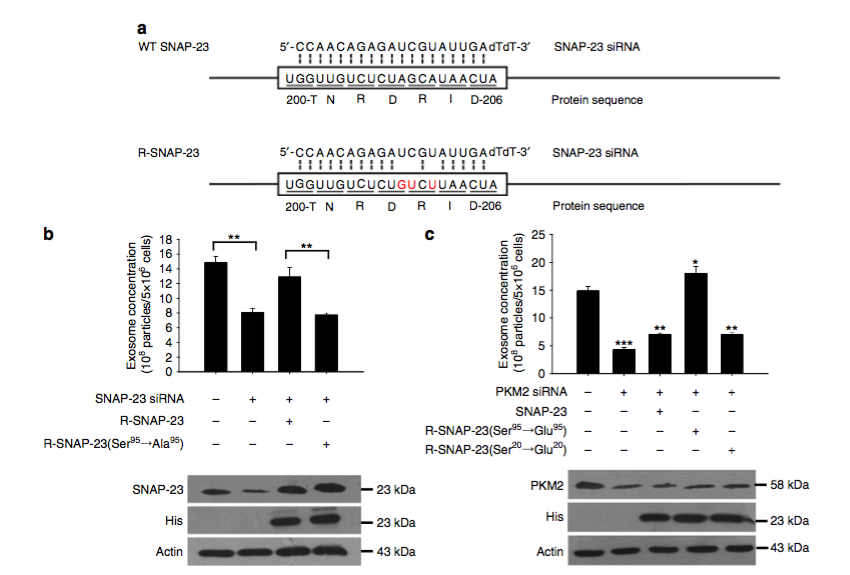
图 3:SNAP23 的 Ser95 磷酸化促进外泌体的释放
参考文献:Wei Y, Wang D, Jin F, Bian Z, Li L, Liang H, Li M, Shi L, Pan C, Zhu D, Chen X, Hu G, Liu Y, Zhang CY, Zen K. Pyruvate kinase type M2 promotes tumour cell exosome release via phosphorylating synaptosome-associated protein 23. Nat Commun. 2017 Jan 9;8:14041.
扫描上面二维码在移动端打开阅读