代谢异常是肿瘤的主要特征之一。近年来不少研究表明肿瘤或机体代谢产物或者代谢通路在肿瘤发生发展中发挥重要作用。在此,小编盘点了近期关于肿瘤代谢的最新研究进展。与大家分享。
【1】新研究揭示表观遗传和代谢如何在癌症发育中发挥作用
DOI: https://doi.org/10.1093/bfgp/elx001
最近一项研究对表观遗传学如何调节人类基因程序进行了研究。该研究表明如果表观遗传受到扰乱就有可能开启癌基因或关闭抑癌基因,这两种事件都会导致正常细胞变成肿瘤细胞引起癌症。
这篇文章提示化学修饰的写入和擦除都要保持一定的平衡,如果这种平衡被打破系统就会出现问题。对于细胞来说,这就意味着细胞会出现无限制生长、发生癌症或死亡。研究人员认为我们对于表观遗传学调控有更好的了解,就可以设计出调节这些因子的药物。
表观遗传组的改变也会帮助肿瘤细胞逃避免疫系统的检测,这也是肿瘤免疫治疗研究想要解决的问题。
总得来说,精准医学结合癌症系统生物学可以揭示基因组和表观遗传组的变化,发现适合药物靶向的一些分子途径。表观遗传的主要调控因子通过两种方式引起癌症:触发癌基因激活和阻止肿瘤抑制因子表达,最终这两种机制促进和推动癌症进展。除此之外,表观遗传变化和代谢产物紧密联系,彼此依赖。代谢产物能够起始、靶向和维持表观遗传,反之亦是如此。表观遗传调控因子还与转录复合体存在相互作用。除此之外还可以利用代谢产物可以靶向、放大或沉默这些应答。
“这可以成为癌症精准靶向治疗的一个范例,表观遗传发生失调的病人可以获益,通过调节表观遗传学还可以克服目前存在的癌症治疗抵抗问题。”文章作者FabianV. Filipp这样说道。
【2】JCI:代谢酶突变或可帮助脑部肿瘤躲避免疫治疗
DOI: 10.1172/JCI90644
神经胶质瘤是最常见的脑肿瘤类型,虽然大多数神经胶质瘤都归类为可治愈类型,这些低级别肿瘤也有可能会发展为更具侵袭性的类型,并且抵抗肿瘤靶向治疗,包括免疫治疗。
在本周发表在国际学术期刊JCI上的一项新研究中,美国UCSF的HidehoOkada实验室研究了异柠檬酸脱氢酶(IDH)发生突变是否会帮助肿瘤抵抗免疫治疗,IDH突变通常出现在低级别的神经胶质瘤中。
研究人员在人类星形胶质细胞和神经胶质瘤小鼠模型上发现,IDH发生突变会通过降低对T细胞的招募抑制T细胞在肿瘤部位的聚集损伤肿瘤微环境中的免疫应答。因此IDH突变或可帮助神经胶质瘤躲避依赖免疫系统激活的抗肿瘤靶向治疗。
重要的是,研究人员在神经胶质瘤小鼠模型上观察到利用突变IDH1的一种特异性抑制剂IDH-135可以逆转突变引起的T细胞聚集受阻,并且抑制突变的IDH能够增强以疫苗为基础的免疫治疗方法。该发现提示联合疗法或能够对抗IDH突变造成的影响,提高神经胶质瘤对免疫治疗的应答情况。
【3】Sci Rep:鉴别出结直肠癌得以继续恶化发展的新型代谢特性
doi:10.1038/srep38415
日前,一项发表在国际杂志ScientificReports上的研究报告中,来自大阪大学的科学家通过研究阐明了结肠癌中谷氨酰胺代谢的重要性;我们都知道谷氨酰胺代谢对于胰腺癌非常重要,但其对于结肠癌发生的重要性研究者却知之甚少,而本文研究就解开了这一谜题。
文章中研究者MasamitsuKonno及其同事通过研究旨在阐明人类结直肠癌中代谢适应性对于癌细胞营养压力的重要性以及其在癌基因表达过程中的角色,研究结果表明,结直肠癌的代谢与胰腺癌中癌细胞的代谢并不相同,这取决于基因组的改变,而此前研究者并未阐明这一结果。
研究者认为结直肠癌的代谢并不仅局限于KRAS的突变,当维持细胞TCA循环活性时在葡萄糖缺失的状况下结直肠癌细胞依然能够存活,而细胞的存活依赖于能量和活性氧产生之间的精细平衡调节,谷氨酸脱氢酶1(GLUD1)和SLC25A13在缺失葡萄糖的情况下扮演着关键角色,同时其还和肿瘤的恶性程度以及结直肠癌患者的预后表现直接相关。
【4】PNAS:延缓衰老的代谢途径也会加速脑癌生长
DOI:10.1073/pnas.1610921114
最近一项研究发现一条延缓衰老的代谢途径可能会促进脑癌发展。
烟酰胺腺嘌呤二核苷酸途径(NAD+途径)在胶质母细胞瘤这种致命脑癌中过度活跃。胶质母细胞瘤是成人中最常见侵袭性最强的一种脑癌,超过70%的胶质母细胞瘤病人在诊断后两年内死亡。
这项新研究发现病情更加严重的患者其肿瘤细胞NAD+途径中一个叫做NAMPT的基因表达水平更高。该基因表达水平升高的肿瘤在移植到小鼠体内之后能够快速生长,而一旦NAMPT表达受到抑制肿瘤就会出现萎缩。
相关研究结果发表在国际学术期刊PNAS上,该研究表明抑制NAD+途径或可改变胶质母细胞瘤病人的病情,但可能也会影响其他生物学过程,比如衰老。
在这项研究中,研究人员利用人类胶质母细胞瘤细胞发现NAMPT能够帮助癌症干细胞存活和增殖,促进肿瘤生长,抑制NAMPT能够降低癌症干细胞自我更新的能力。除此之外他们还发现胶质母细胞瘤会通过增强NAD+途径上一些基因的表达应对放射治疗,在放疗之前抑制NAMPT能够让癌细胞更容易被杀死。
NAD+途径中包括许多不同基因和蛋白,研究人员认为如果能够小心调节该途径有望既达到抑制癌症发展的目的又不会加速衰老或影响其他重要生物学过程。
【5】Cancer Res:人群研究发现代谢紊乱因素与肝癌风险相关
DOI:10.1158/0008-5472.CAN-16-0787
在一项大型前瞻性群组研究中,来自美国国家癌症研究所的研究人员发现高BMI,大腰围以及2型糖尿病都与肝癌风险增加存在相关性。相关研究结果发表在国际学术期刊CancerResearch上。
研究人员表示,从上世纪70年代中期开始,美国的肝癌发生率不断增加,并且肝癌病人的预后情况特别严峻。考虑到美国肥胖的发生率也在不断增加,因此他们研究了肥胖以及2型糖尿病是否与肝癌风险有关,研究数据来自14项针对美国成年人进行的不同研究。
参与这14项不同研究的157万美国成年人在调查问卷中回答了关于身高、体重、饮酒和吸烟情况以及其他可能的癌症风险因素的问题。参与研究时并未有参与者患癌,6.5%的参与者患有2型糖尿病,之后共有2162名参与者患上肝癌并且得到了研究人员的证实。
研究人员在肥胖及糖尿病患者和健康群组中比较了肝癌发生率,想要确定影响肝癌发生的相关风险因素。结果发现BMI每增加5kg/m2,男性和女性发生肝癌的风险分别增加38%和25%;腰围每增加5cm,肝癌风险就会增加8%。在矫正了饮酒、吸烟、种族和BMI之后,2型糖尿病患者患肝癌的风险是非糖尿病人群的2.61倍,并且风险随BMI增加而升高。
研究人员表示,BMI、腰围和2型糖尿病这三个因素与肝癌风险存在非常显著的相关性,这进一步表明肝癌是肥胖相关癌症名单中的一员。该研究还提示人们应当为对抗肥胖投入更多关注。
【6】Nat Cell Biol:科学家找到控制前列腺癌进展和转移的代谢总开关
doi:10.1038/ncb3357
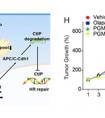
最近,来自西班牙的科学家们在国际学术期刊Nature CellBiology上发表了一项最新研究进展,他们发现一种参与代谢的转录共激活因子能够抑制前列腺癌进展和转移,这为找到对抗前列腺癌的新方法提供了重要方向。
在这项最新研究中,研究人员设计了一种生物信息学分析方法整合多个前列腺癌数据集的数据发现转录共激活因子PGC1α在前列腺癌中发生表达下调,并且此现象与疾病进展具有相关性,因此研究人员提出PGC1α或抑制前列腺癌进展和转移。随后研究人员构建了基因工程小鼠模型和异种移植模型,通过一系列实验证明PGC1α确实能够对抗前列腺癌进展和转移。
研究人员还从机制上进行了深入分析,他们结合代谢组学和转录组学方法发现PGC1α能够激活雌激素相关受体α(ERRα)依赖性的转录程序,诱导细胞处于一种分解代谢状态,从而抑制癌症转移。研究人员还发现基于PGC1α-ERRα途径的基因表达特征在前列腺癌的诊断方面具有一定潜力。
这项研究结合生物信息学分析,组学分析和动物模型等方法发现在代谢中发挥重要作用的转录共调节因子PGC1α能够抑制前列腺癌进展和转移,为开发治疗前列腺癌的新方法提供了重要信息。
【7】Cell Metab:科学家找到白血病细胞的代谢“命门”
DOI: http://dx.doi.org/10.1016/j.cmet.2016.03.008
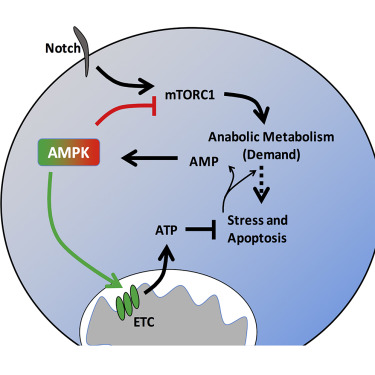
近日,来自美国杜克大学的研究人员在国际学术期刊cell metabolism上发表了一项最新研究进展,他们发现糖酵解在T-ALL细胞中受到一定限制,并发现Notch信号会通过激活AMPK促进癌细胞存活,这对于该类型白血病的治疗具有一定提示。
T细胞急性淋巴细胞白血病是一种侵袭性非常强的恶性疾病,该病的发生常与Notch信号途径中发生的突变有关。之前研究发现正常激活的T细胞和癌化T细胞都能够使用有氧糖酵解支持细胞增殖,但是这两类T细胞在代谢方面究竟存在多大程度的相似性,以及两者之间的差异是否能够揭示T-ALL的代谢弱点仍然不清楚。
在这项研究中,研究人员发现相比于处于增殖状态的正常T细胞,T-ALL细胞内有氧糖酵解的活跃度明显更低,并且两者存在明显的代谢差异。研究人员发现Notch信号能够促进T-ALL细胞的糖酵解,导致代谢应激增加,进而激活AMPK分子。与正常激活的T细胞不同,T-ALL细胞内AMPK会通过抑制mTORC1分子明显限制有氧糖酵解过程,但同时存在氧化代谢和线粒体复合体I的活性增强。
研究人员在文章中表示,最为重要的是他们发现AMPK缺失或抑制复合体I的活性能够导致T-ALL细胞发生死亡,降低疾病负担。因此他们认为AMPK能够抑制合成代谢生长信号,同时通过促进线粒体内的信号途径,减轻代谢应激和细胞凋亡,从而对T-ALL细胞的存活具有非常重要的意义。这项研究对于T-ALL 疾病的药物开发和治疗具有一定提示意义。
【8】JCB:关键代谢通路如何促进乳腺癌转移
doi:10.1083/jcb.201510002
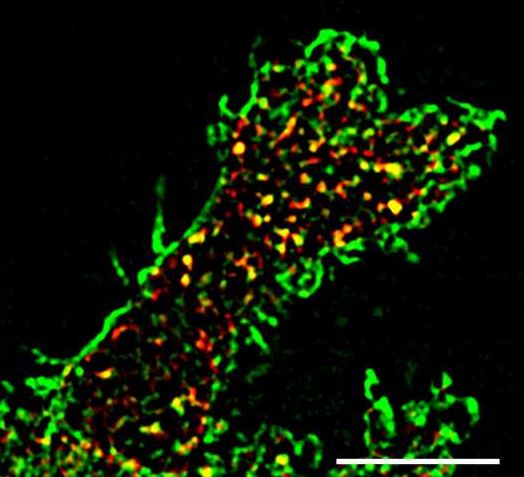
发表于国际杂志the Journal of Cell Biology上的一项研究论文中,来自北海道大学医学院的研究人员通过研究发现,在特定乳腺癌中被上调的一种特殊代谢通路或可通过激活细胞信号蛋白Arf6来促进疾病的恶化,研究者表示,这项题为“P53- and mevalonate pathway-driven malignancies require Arf6 for metastasis and drug resistance”的研究报告表明,他汀样的药物或可有效治疗那些机体中Arf6信号蛋白高表达的乳腺癌患者。
甲羟戊酸途径(MVP)是一种特殊的代谢通路,其可以帮助产生组成一系列生物性分子的基本元件,包括从胆固醇到长链脂质分子等;而肿瘤抑制因子p53的突变就会上调MVP,这种现象就可以增强某些乳腺癌细胞系的侵袭力,研究者推测,MVP途径或可通过激活Arf6信号通路来促进癌细胞的侵袭性,而这就可以通过促进细胞向其它能动状态过渡进而增强癌细胞的转移和侵袭力。
研究者Hisataka Sabe表示,我们发现MVP可以促进Arf6蛋白向质膜的募集,而在质膜中Arf6就会被受体酪氨酸激酶所激活,而MVP通路就是通过产生特殊的脂质基团来完成这项任务,这种特殊的脂质基团可以蛋白Rab11b锚定到细胞膜上,从而促进Rab11b将Arf6蛋白运输到激活位点,而抑制Rab11b就会减少乳腺癌细胞系MDA-MB-231的侵袭力,这种特殊的乳腺癌细胞系可以产生大量的Arf6信号蛋白。
Arf6通路还可以增强乳腺癌细胞对药物的耐受性,研究者指出,抑制Rab11b或者名为EPB41L5的Arf6通路组分,就可以提高MDA-MB-231细胞对两种不同细胞毒性化合物的敏感性。他汀类药物可以抑制HMG-CoA还原酶(羟甲基戊二酸单酰辅酶a还原酶),该还原酶是MVP中的关键组分,他汀类药物原本用作降胆固醇之用,此前研究者还调查这种药物是否可以作为一种潜在的抗癌药物,但截至目前为止临床结果好坏参半。
本文的研究结果重点关注机体中Arf6信号蛋白高表达的乳腺癌患者,药物辛伐他汀可以增加MDA-MB-231细胞的药物敏感性,同时抑制细胞的转移能力。最后研究者Sabe说道,阻断MVP通路或可有效杀灭过表达Arf6蛋白的癌细胞,因此开发特殊的治疗方法就显得非常重要,因为研究者目前发现一些机体中肿瘤MVP组分和Arf6信号蛋白高表达的患者的长期生存率发生了明显下降。(生物谷Bioon.com)
扫描上面二维码在移动端打开阅读