药品概述
2020年5月14日,武田中国宣布旗下靶向创新药物安适利®(注射用维布妥昔单抗)经国家药品监督管理局正式批准进入中国,获批适应症为成人CD30阳性的复发或难治性系统性间变性大细胞淋巴瘤(sALCL)和 复发或难治性经典型霍奇金淋巴瘤(cHL)的治疗。
美国FDA获批的其他适应证:先前接受过系统治疗的原发性皮肤间变性大细胞淋巴瘤或CD30阳性蕈样真菌病成人患者;联合化疗治疗初治Ⅲ或Ⅳ期经典型霍奇金淋巴瘤、初治系统性间变性大细胞淋巴瘤或其他表达CD30的外周T细胞淋巴瘤患者。
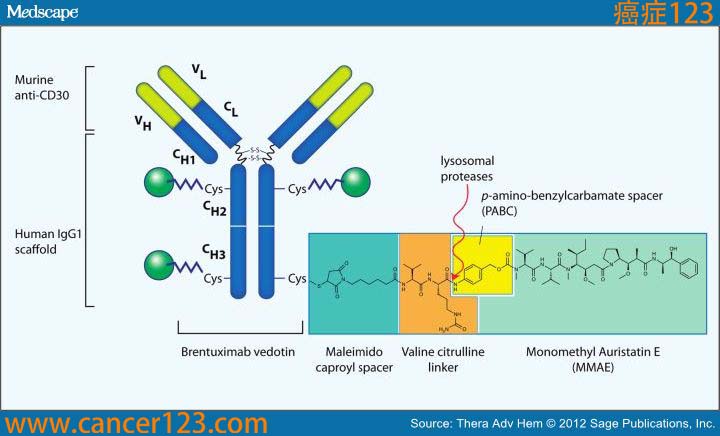
安适利(注射用维布妥昔单抗)由靶向CD30的单克隆抗体连接一种抑制微管的细胞毒药物(单甲基澳瑞他汀E,MMAE)组成,可在血液中稳定存在,精准杀灭表达CD30的肿瘤细胞。该产品临床使用经验丰富,真实世界循证依据充分,疗效久经验证。此前,美国国家综合癌症网络(NCCN)指南已将维布妥昔单抗推荐为标准治疗药物,中国临床肿瘤学会(CSCO)指南亦将其纳入临床选择范围。
简要说明书
| 维布妥昔单抗Brentuximab (ADCETRIS,安适利®)说明书 | |
| 药物: | 维布妥昔单抗注射液 Brentuximab (ADCETRIS,安适利®) |
| 中国上市情况: | 已上市 |
| 治疗: | 成人CD30阳性的复发或难治性系统性间变性大细胞淋巴瘤(sALCL)和 复发或难治性经典型霍奇金淋巴瘤(cHL)的治疗。 |
| 参考用法用量: | 推荐剂量为 1.8 mg/kg, 30 分钟以上静脉输注给药,每 3 周 1 次。 |
| 不良反应: | 发热性中性粒细胞减少症,急性胰腺炎和胃肠道并发症,丙氨酸氨基酸转移酶(ALT)和天冬氨酸氨基酸转移酶(AST)升高,PML,高血糖,非感染性肺毒性,包括肺炎,间质性肺病和 ARDS,Stevens-Johnson 综合征,中毒性表皮坏死松解症,包括致死性结局,外渗相关反应。 |