在过去的 2 年中,研究人员、生物制药公司和投资者对肿瘤免疫学领域产生了巨大的兴趣。值得注意的是,免疫检查点抑制剂被广泛认为是肿瘤免疫治疗的第一波方案,已经对黑色素瘤患者显示出显著生存效益,并且其益处逐步扩展到另外五种癌症适应症。目前,单是程序性细胞死亡蛋白 1(PD1)和其配体 PD-L1 为靶标免疫检查点抑制剂,就有近千个正在进行的临床试验,FDA 已经为这些产品授予了 13 个突破性疗法认定。行业内众多人士预测,到 2025 年,肿瘤免疫学市场的价值将高达 450 亿到 1000 亿美元。

最近《Nature Reviews Drug Discovery》发表了一篇有关这一领域的论文,为我们介绍了五个肿瘤免疫疗法的常见误区,并提供了一个直面事实与挑战的全新视角。
误区 1. 单靠肿瘤学免疫方法就可以治愈癌症。
事实:尽管最初的临床结果充满希望,但并非所有肿瘤类型都对免疫检查点抑制剂有反应。甚至在一些 “免疫原性(immunogenic)” 肿瘤类型中,患者群体的无应答率高达 40%~60%左右。然而,免疫肿瘤药物被逐步定位成为大多数肿瘤类型的骨干治疗方案,诸多大型制药公司均在该领域有所部署,相继有产品和在研管道进入市场(图 1)。
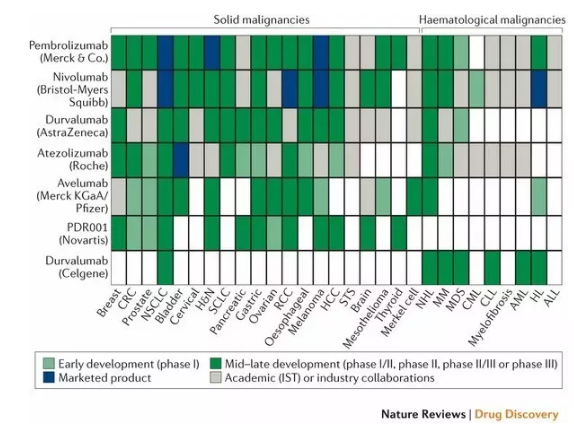
▲各个主要抗 PD1/PD-L1 疗法研发项目对癌症适应症的覆盖(图片来源:《Nature Reviews Drug Discovery》)
误区 2. 进入肿瘤免疫学市场需要超过 10 亿美元的最低投资额。
事实:基于现有临床试验数量和类型的粗略估计,阿斯利康、百时美施贵宝、默沙东和罗氏各自在 2016 年输出了高达 10 亿美元的资金用于肿瘤免疫药物的开发。然而,利用更集中的发展战略,后来进入这一领域的企业可能不一定需要投入太多。特别是新的或小的制药公司可以采取以下各种策略:
• 瞄准跨多种组合和适应症的临床研究。百时美施贵宝、默沙东和罗氏等早期进入者有广泛的发展计划。其他的公司可以考虑使用适应性试验设计和合作伙伴关系来获得组合和适应症的广度。
• 注重生物学机制或生物标志物开发层面的深度。例如,诺华公司通过购买 CoStim 公司,获得了两个领域内首个(first-in-class)免疫检查点抑制剂以启动其第一个人体试验。领军者和挑战者正在使用基于 PD-L1 的临床试验来确定失败机制和生物标志物,迈向新的组合目标。
• 强调下一代治疗手段和技术。例如,葛兰素史克公司出售了其肿瘤组合,通过与 Adaptimmune 合作 T 细胞疗法,来集中表观遗传学和下一代免疫肿瘤学的早期研发。
• 投资于具有较大潜力和份额的适应症。例如,Celgene 建立了多个合作伙伴关系,努力在血液 / 肿瘤学建立一个免疫肿瘤学项目,该领域已经拥有强大的市场。
误区 3. 面对大的适应症时,总有进入市场的空间。
事实:进入非小细胞肺癌适应症这样的大型市场可能看起来很有吸引力,因为即使一小部分市场也有可能产生较大收益。然而随着市场逐渐拥挤,市场区分对后继进入者来说入门条件太高:临床上需要显示更高的功效或安全性;市场上则需要强大的销售力量和良好公关。最后,竞争患者招募也可能对后期进入者提出挑战。
误区 4. 检查点抑制剂很快就会被基因编辑所掩盖。
事实:精确进行基因编辑的能力激发了医疗、科学和投资界的巨大热情,尤其是通用型细胞治疗所带来的希望。然而,基于基因组编辑的肿瘤学方法进入主流仍需要 8-10 年的光景。例如,第一个基于 CRISPR-Cas9 技术的美国临床试验最近才获得批准。而同时,免疫肿瘤学方法会成为许多肿瘤类型治疗的黄金标准。
误区 5. 已经建立的癌症治疗(如放射治疗、化疗和靶向药物)将被肿瘤免疫学疗法完全替代。
事实:虽然免疫检查点抑制剂变成几种适应症新的护理标准,但对于许多其他适应症,肿瘤免疫学方法预期将主要发挥补充作用。很明显,涉及 PD1 或 PD-L1 抑制剂的约 700 多种临床组合中超过 50%在试验臂上与 “化学放射” 或建立的靶向试剂配对(图 2)。

▲图二:领先药企正在进行的肿瘤免疫学疗法组合试验(图片来源:《Nature Reviews Drug Discovery》)
前进道路上的挑战
鉴于目前令人印象深刻的早期临床结果,联合治疗将成为未来的主要方向。事实上,各家公司越来越多地追求组合,甚至在一线治疗设置上。然而广泛的组合方案将需要强大的科学基础,明确对患者进行亚分段和设计创新的适应性试验。这有望带来领域首个组合(first-in-combo)和领域最佳组合(best-in-combo)之类的新概念。
关注生物标志物确定的更窄患者人群也是有必要的。由于部分 PD-L1 阴性患者对 PD1 或 PD-L1 抑制剂有反应,如何看待生物标志物和伴随诊断的相关有效性在整个领域仍有争议。事实上也很对,PD-L1 只是复杂动态免疫系统中许多检查点分子之一。再接下来的新一代治疗挑战中,我们期望在治疗之前和之后能够利用肿瘤进行免疫配制来限定新的患者区段,并确定免疫检查点抑制剂是否可作为潜在的组合骨架或辅助疗法。
我们相信,众多患者将会从免疫疗法中受益,并获得越多、越好的护理。
相关会议推荐: 第四届肿瘤基础和转化医学前沿国际研讨会 4月21-23 贵阳
扫描上面二维码在移动端打开阅读