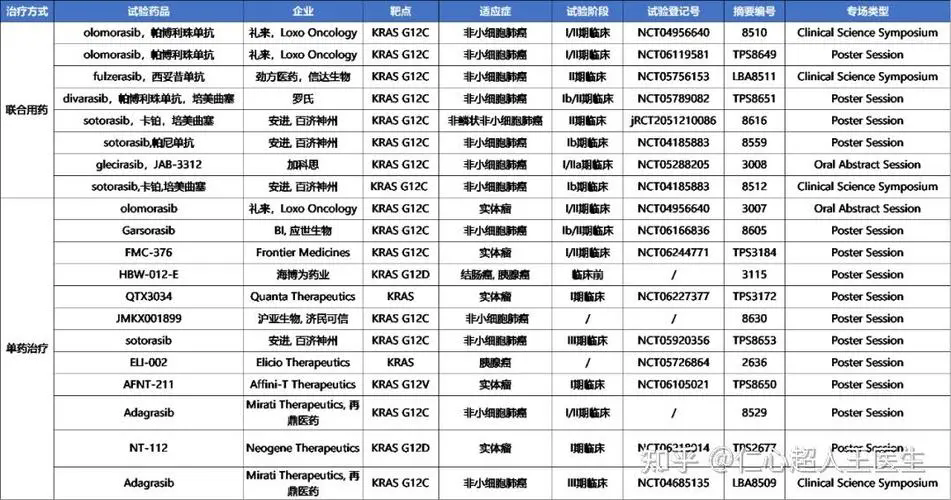
大约一周前,一个大学好友突然告诉我,他父亲被诊断为肺癌。他看我朋友圈都是些重磅进展,就问我是不是知道有效的治疗方法。在一番问候之后,我问他有没有让他父亲做基因检测,他说有这个打算。然后我让他赶紧带爸爸去做,同时给他说了一堆靶向治疗药物,以及Merck的Keytruda,和罗氏的Tecentriq。
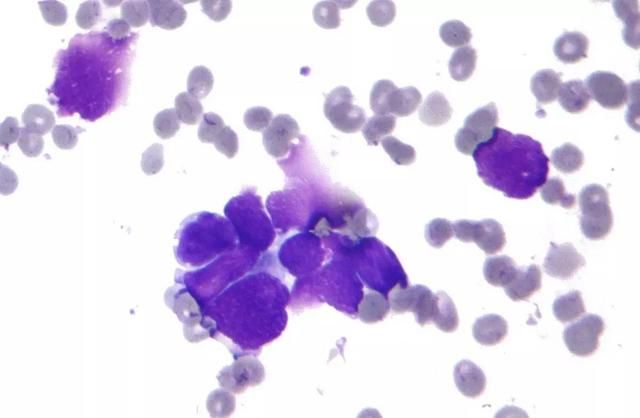
他沉默了一会儿,然后告诉我他父亲患的是晚期小细胞肺癌,已经出现耐药了。小细胞肺癌!为啥偏偏是小细胞肺癌。
实际上,小细胞肺癌是被列入疑难杂症之列的大魔头,因为这个发病率占所有肺癌15%左右的「小众」癌种,导致的死亡竟然占到所有肺癌的25%以上,一旦确诊,5年存活率小于5%(Joshi et al. 2013)。更可怕的是,治疗小细胞肺癌已经近40年没有新的疗法出现了,所有的靶向药物都没有取得成功(Sharp et al. 2016)。目前治疗复发性小细胞肺癌,只有GSK在2007年获得FDA批准的化学药物topotecan。
2002年,一场类似的对话发生在Brian Slingerland和Scott Dylla之间。Slingerland的两个亲人因为癌症离世,其中一位患的就是小细胞肺癌。Slingerland问在研究肿瘤的Dylla博士,「癌症能治愈吗?」Dylla说,「可以,我们只需摧毁肿瘤干细胞。」
六年之后的2008年,为了治愈癌症的梦想,有金融学背景的Slingerland,拉着肿瘤学专家Dylla(任首席科学官)和拥有MBA的Daniel T. Reiner,三人在美国湾区共同组建了Stemcentrx,他们想通过消灭肿瘤干细胞治愈癌症。对于一家初创公司而言,这个想法是疯狂的,因为肿瘤干细胞学说在学界还存在较大争议,并没有形成共识。这是一场狂赌。
然而,与他们治疗癌症的疯狂想法相比,他们做事的风格却极其低调。在2015年之前,很少有人知道Stemcentrx的存在,因为他们没有官方网站,也没有新闻报道。然而,即使是低调如Stemcentrx的公司,还是吸引了大神Peter Thiel的关注,Thiel下辖的Founders Fund给Stemcentrx投了2亿美元,是Thiel在其他25家生物技术公司投资总额的3倍。2015年8月,Stemcentrx又获得由Fidelity领投的2.5亿美元,市值飙升到50亿美元。几乎所有人都认为Stemcentrx离IPO不远了。

Scott Dylla博士(图:researchgate.net)
巨额融资的背后,是他们踏实的科学研究。Dylla带领公司科研团队找到了小细胞肺癌的肿瘤干细胞标志物DLL3蛋白(成人的健康细胞表面没有,肿瘤干细胞表面有),并成功研发出靶向该蛋白的药物SC16LD6.5(Rovalpituzumab tesirine,Rova-T)。2015年8月,Dylla团队在《科学》旗下著名期刊《转化医学》发表了他们这一重磅研究成果(Saunders et al. 2015)。实际上,他们已经在两年前就默默地开启了I期临床研究。
Rova-T是一种抗体药物偶联物(antibody-drug conjugate ,ADC),是单克隆抗体与毒素(Pyrrolobenzodiazepines)的结合物,抗体负责结合表面携带DLL3蛋白的肿瘤干细胞,毒素负责破坏癌细胞的DNA,最终导致肿瘤干细胞死亡。Dylla在论文中表示,Rova-T可以有效的靶向并摧毁DLL3蛋白表达量高的肿瘤起源细胞(Tumor-initiating cells ,TICs;包括肿瘤干细胞在内),是治疗小细胞肺癌的全新药物(first-in-class)。这一研究也初步证明利用肿瘤干细胞学说治疗癌症或许是可行的。
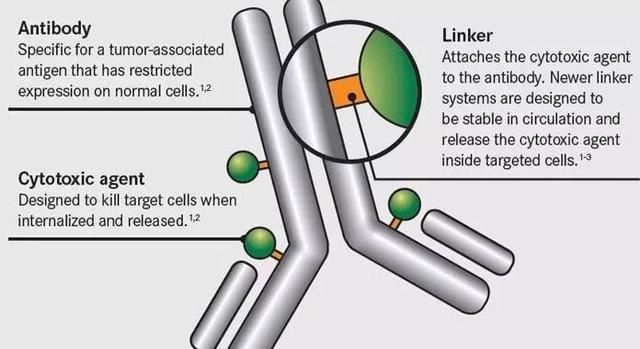
抗体药物偶联物示意图(图:http://molecularbiologynews.org/)
于此同时,于2013年7月开启的Rova-T治疗小细胞肺癌I期临床研究,82名志愿者全部入组,其中有74名患者是小细胞肺癌患者。在此期间,Stemcentrx也在断断续续公布一些初步的临床数据,这也大大的促进了它融资的进程。
2016年4月28日,在外围对Stemcentrx垂涎已久的制药巨头AbbVie对外宣布,AbbVie将斥资58亿美元收购由风险投资支撑的Stemcentrx,以加强AbbVie的抗癌药物组合。如若Stemcentrx的药物达到里程碑,将会有另外40亿美元入账。据悉,这是风投支撑公司历史上第二大收购案。交易完成之后,风投大神Thiel和他的基金收获17亿美元。

Stemcentrx的生产车间(图:technologyreview.com)
如果说Slingerland和Dylla创办Stemcentrx是狂赌,那AbbVie此次斥巨资收购的疯狂之举,简直找不到合适的词来形容。风险之大,可想而知。
今年1月初,顶级医学期刊《新英格兰医学期刊》全文刊登了Rova-T治疗小细胞肺癌的I期临床研究结果(Rudin et al. 2016)。虽然这个I期临床研究主要是为了检验Rova-T的安全性和有效剂量,但是里面隐含的初步数据还是让AbbVie和小细胞肺癌患者看到了一线希望。
本次历时近3年临床研究,由纪念斯隆-凯特琳癌症中心的Charles M Rudin教授领导。一共招募了74名小细胞肺癌患者,这些志愿者在进组前均接受了一线或者二线治疗。研究表明,患者对Rova-T的最大耐受为每3周0.4mg/kg。根据这个结果,Rudin教授团队认为,在后续的II期临床实验中,推荐给药量为每6周0.3mg/kg。

Charles M Rudin教授(图:vimeo.com)
既然已经证明Rova-T是安全的,而且找到了合适的给药量。那是不是可以稍稍利用下这次的临床数据,窥探一下Rova-T是不是真的有效呢?
于是,Rudin教授团队结合研究成果,和患者的用药情况,发现有60名患者的给药量在推荐给药的有效范围之内。于是Rudin教授团队就利用这部分数据对Rova-T的疗效做了个整体的评估。他们发现,有11名患者(18%)有明确的客观响应(肿瘤缩小),41名患者(68%)的疾病得到了控制(肿瘤不再变大)。中位无进展生存期为2.8个月(2.5-4.0),中位总生存期为4.6个月(3.9-7.1)。在随访一段时间后,Rudin教授团队发现39名对化疗敏感的患者1年存活率为17%,30名对化疗产生耐药性的患者1年存活率在21%左右。
既然是靶向DLL3蛋白的药物,研究人员最关心的还是DLL3蛋白高表达(50%的肿瘤细胞表面出现DLL3蛋白)的患者的表现?于是Rudin教授团队又从这74名患者中找出了给药量在有效范围之内,且DLL3蛋白高表达的小细胞肺癌患者,一共是26名。
在这26名DLL3蛋白高表达的患者中,10名患者(38%)具有确定的客观反应,23名患者(88%)病情得到了控制,无进展生存期为4.3个月(2.8-5.6),中位总生存期为5.8个月(4.4-11.6)。
而在8名DLL3蛋白低表达患者的小亚组中,没有患者对Rova-T表现出明确的客观响应,只有4名患者(50%)病情得到了控制,中位无进展生存期为2.2个月(1.3-2.5 ),中位总生存期为2.7个月(1.2-10)。
显然,从初步的数据来看,尽管治疗效果不是特别sexy,Rova-T还是值得期待的。尤其是在比较DLL3蛋白高表达的患者与DLL3蛋白低表达的患者对Rova-T的反应时,证明DLL3蛋白的确是小细胞肺癌的潜在标志物。这的确给小细胞肺癌的治疗指出了一个新的方向。
据AbbVie透露,它正在向FDA给Rova-T申请各种称号。同时AbbVie还与BMS展开合作,计划利用免疫检查点抑制剂Opdivo与Rova-T联合治疗小细胞肺癌。如果没有意外的话,乐观预计Rova-T会在2018年面市。(生物谷Bioon.com)
参考资料:
Joshi, M., (2013). Small-Cell Lung Cancer: An Update on Targeted Therapies. Impact of Genetic Targets on Cancer Therapy. W. S. El-Deiry. New York, NY, Springer New York: 385-404.
Rudin, C. M., (2016). Rovalpituzumab tesirine, a DLL3-targeted antibody-drug conjugate, in recurrent small-cell lung cancer: a first-in-human, first-in-class, open-label, phase 1 study. The Lancet Oncology 18(1): 42-51.
Saunders, L. R., (2015). A DLL3-targeted antibody-drug conjugate eradicates high-grade pulmonary neuroendocrine tumor-initiating cells in vivo. Science Translational Medicine 7(302): 302ra136-302ra136.
Sharp, A., (2016). Development of molecularly targeted agents and immunotherapies in small cell lung cancer. European Journal of Cancer 60: 26-39.
扫描上面二维码在移动端打开阅读